题目内容
10.下列叙述不正确的是( )| A. | 常温下,在$\frac{c(H+)}{c(OH-)}$=1012的溶液中,Fe2+、I-、NO3-、Cl-一定不能大量共存 | |
| B. | H2A是二元弱酸,常温下,0.1mol/LNaHA溶液的pH约为5,说明HA-电离程度大于水解程度 | |
| C. | 使用催化剂一定能够降低化学反应的反应热(△H) | |
| D. | NA为阿伏加德罗常数的值,常温常压下,28gC2H4和C3H6混合气体含有的原子数为6NA |
分析 A、常温下,在$\frac{c(H+)}{c(OH-)}$=1012的溶液中,呈酸性,而Fe2+、NO3-在酸性溶液中不能共存;
B、0.1mol/LNaHA溶液的pH约为5,溶液呈酸性;
C、使用催化剂只改变反应的速率,而反应物和生成物的总能量不变;
D、C2H4和C3H6最简式相同CH2,依据n=$\frac{m}{M}$计算28 gCH2物质的量,得到原子数;
解答 解:A、常温下,在$\frac{c(H+)}{c(OH-)}$=1012的溶液中,呈酸性,而Fe2+、NO3-在酸性溶液中不能共存,生成铁离子和氮的氧化物,故A正确;
B、0.1mol/LNaHA溶液的pH约为5,溶液呈酸性,说明HA-电离程度大于水解程度,故B正确;
C、使用催化剂只改变反应的速率,而反应物和生成物的总能量不变,所以该反应的反应热不变,故C错误;
D、C2H4和C3H6最简式相同CH2,28 gCH2物质的量=$\frac{28g}{14g/mol}$=2mol,所以混合气体含有的原子数为6NA,故D正确;
故选C.
点评 本题是一道关于离子共存、催化剂与反应热的关系以及电解质在水中的电离等方面知识的综合考查题,难度较大.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
20.将5.4gAg投入一定量的浓硝酸中完全溶解得到NO和NO2的混合气体,用NaOH溶液把该混合气体完全吸收得到NaNO3和NaNO2的混合溶液,则所得NaNO2的物质的量为( )
| A. | 0.024mol | B. | 0.006mol | C. | 0.075mol | D. | 0.3mol |
18.一种碳纳米管新型二次电池的装置如图所示,下列说法中正确的是( )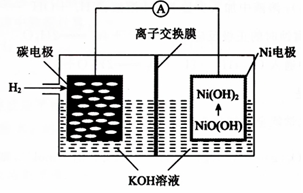

| A. | 离子交换膜选用阳离子交换膜(只允许阳离子通过) | |
| B. | 正极的电极反应为NiO(OH)+H2O+e-═Ni(OH)2+OH- | |
| C. | 导线中通过1mol电子时,理论上负极区溶液质量增加1g | |
| D. | 充电时,碳电极与电源的正极相连 |
5.《天工开物》对某种颜料“朱”制备的描述为:“夫亦依坎附离,而共呈五行变态.”所述“朱”的制备,用水银一斤和过量的硫(石亭脂)进行反应,得到上朱十四两、次朱三两五钱,共得朱十七两五钱(当时一斤等于十六两).有关该反应的描述正确的是( )
| A. | “朱”的主要成分是Hg2S | B. | 该反应为置换反应 | ||
| C. | 该反应不符合质量守恒定律 | D. | 该反应Hg作还原剂 |
20.下列图象与对应叙述相符合的是( )
| A. | 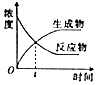 图表示某可逆反应物质的浓度随时间的变化,且在t时刻达到平衡状态 | |
| B. | 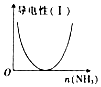 图表示向CH3COOH溶液中通入NH3至过量的过程中溶液导电性的变化 | |
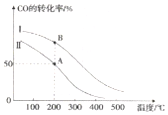
| C. |  图表明合成氨反应时放热反应,b表示在反应体系中加入了催化剂 | |
| D. | 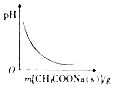 图表示向CH3COOH溶液中逐渐加入CH3COONa固体后,溶液pH的变化 |
16.下列物质属于氧化物的是( )
| A. | Cl2O | B. | H2SO4 | C. | C2H5OH | D. | KNO3 |
 甲醇汽油是一种新能源清洁燃料,可以作为汽油的替代物.有关反应的热化学方程式如下:
甲醇汽油是一种新能源清洁燃料,可以作为汽油的替代物.有关反应的热化学方程式如下: