题目内容
下列配制的溶液浓度偏高的是( )
| A、配制盐酸溶液用量筒量取盐酸时,俯视刻度线 |
| B、配制盐酸溶液定容时,仰视容量瓶刻度线 |
| C、称量11.7gNaCl配制0.2mol?L-1NaCL溶液1 000mL时,砝码错放左盘 |
| D、NaOH溶解后未经冷却即注入容量瓶定容至刻度线 |
考点:溶液的配制
专题:实验评价题
分析:根据c=
分析操作对溶质的物质的量或对溶液的体积是否有影响判断,如果n偏大或V偏小,则所配制溶液浓度偏高.
| n |
| V |
解答:
解:A、用量筒量取盐酸时俯视刻度线,所取盐酸的体积偏少,溶质的质量偏少,导致配制溶液的浓度偏低,故A错误;
B、定容时,仰视容量瓶刻度线,溶液的体积偏大,导致配制溶液的浓度偏低,故B错误.
C、称量11.7gNaCl固体时用到游码,砝码错放左盘,会导致所称量的NaCl固体的质量偏小,所配制溶液的浓度偏低,故C错误.
D、NaOH固体溶于水放热,故NaOH溶解后未经冷却即注入容量瓶配制导致溶液的体积偏小,配制溶液的浓度偏高,故D正确.
故选D.
B、定容时,仰视容量瓶刻度线,溶液的体积偏大,导致配制溶液的浓度偏低,故B错误.
C、称量11.7gNaCl固体时用到游码,砝码错放左盘,会导致所称量的NaCl固体的质量偏小,所配制溶液的浓度偏低,故C错误.
D、NaOH固体溶于水放热,故NaOH溶解后未经冷却即注入容量瓶配制导致溶液的体积偏小,配制溶液的浓度偏高,故D正确.
故选D.
点评:本题考查配制一定物质的量浓度的溶液的误差分析,题目难度中等,注意根据c=
分析不当操作对n或V的影响.
| n |
| V |

练习册系列答案
相关题目
现有两种只含C、H两种元素的有机物混合气体0.1mol,完全燃烧生成0.12molCO2和0.2molH2O,则该混合气体中( )
| A、一定含有甲烷 |
| B、一定含有乙烯 |
| C、可能含有甲烷 |
| D、不能确定 |
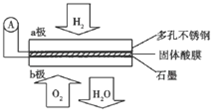 某固体酸燃料电池以Ca(HSO4)2固体为电解质传递H+,其基本结构如图,电池总反应可表示为:2H2+O2═2H2O,下列有关说法正确的是( )
某固体酸燃料电池以Ca(HSO4)2固体为电解质传递H+,其基本结构如图,电池总反应可表示为:2H2+O2═2H2O,下列有关说法正确的是( )| A、电子通过外电路从b极流向a极 |
| B、b极上的电极反应式为:O2+2H2O+4e-═4OH- |
| C、每转移0.1mol电子,消耗1.12L的H2 |
| D、H+由a极通过固体酸电解质传递到b极 |
下列说法正确的是( )
A、按系统命名法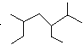 的名称为2-甲基-3,5-二乙基己烷 的名称为2-甲基-3,5-二乙基己烷 |
| B、用Na2CO3溶液能区分CH3COOH、CH3CH2OH、苯、硝基苯四种物质 |
| C、若两种二肽互为同分异构体,则二者的水解产物一定不相同 |
| D、等质量的甲烷、乙烯、1,3-丁二烯分别充分燃烧,所耗用氧气的量依次增加 |
对相同质量的N2与NO作比较,正确的是( )
| A、所含的分子数相等 |
| B、在同温同压下,V(N2)═V(NO) |
| C、所含的原子数不相等 |
| D、在同温同体积下,p(N2)<p(NO) |
欲将含有盐酸的CaCl2溶液中和至中性,在不用指示剂的条件下,最好加入下列物质中的( )
| A、氨水 | B、碳酸钠粉末 |
| C、NaOH溶液 | D、石灰石粉末 |
一种新型熔融盐燃料电池具有高发电效率.现有Li2CO3和Na2CO3的熔融盐混合物作电解质,一极通CO气体,另一极通O2和CO2混合气体,其总反应为:2CO+O2=2CO2.则下列说法中正确的是( )
| A、通CO的一极是正极 |
| B、负极发生的电极反应是:CO+CO32--2e-=2CO2 |
| C、正极发生氧化反应 |
| D、CO32-向正极定向移动 |
25℃时,有pH=3的盐酸和醋酸溶液,下列说法正确的是( )
| A、两种溶液中由水电离出来的c(H+)不相同 |
| B、中和相同体积的两种酸溶液所需NaOH的物质的量相同 |
| C、将两溶液等体积混合,c(H+)>c(CH3COO-)═c(Cl-)>c(OH-) |
| D、分别用燕馏水稀释m倍和n倍,若两溶液pH仍相同,则m<n |
下列化学用语正确的是( )
| A、乙烯的结构简式:CH2CH2 |
B、氯化钠的电子式: |
| C、明矾的化学式:KAlSO4?12H2O |
| D、淀粉的分子式:(C6H10O5)n |