题目内容
现有两种只含C、H两种元素的有机物混合气体0.1mol,完全燃烧生成0.12molCO2和0.2molH2O,则该混合气体中( )
| A、一定含有甲烷 |
| B、一定含有乙烯 |
| C、可能含有甲烷 |
| D、不能确定 |
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:先根据混合物的物质的量、二氧化碳、水的物质的量计算出混合物的平均分子式,然后根据计算结果进行讨论,从而得出该有机混合物的组成情况.
解答:
解:只含C、H两种元素的有机物混合气体0.1mol,完全燃烧生成0.12molCO2和0.2molH2O,
则该混合气体中平均含有的C、H原子数为:
=1.2、
=4,
混合气体的平均分子式为:C1.2H4,
碳原子数小于1.2的烃只有甲烷,所以混合气体中一定含有甲烷,所以A正确,C、D错误;
由于甲烷分子中含有4个H原子,则另一种烃中一定含有4个H原子,可能为乙烯、丙炔,所以B错误;
故选A.
则该混合气体中平均含有的C、H原子数为:
| 0.12mol |
| 0.1mol |
| 0.2mol×2 |
| 0.1mol |
混合气体的平均分子式为:C1.2H4,
碳原子数小于1.2的烃只有甲烷,所以混合气体中一定含有甲烷,所以A正确,C、D错误;
由于甲烷分子中含有4个H原子,则另一种烃中一定含有4个H原子,可能为乙烯、丙炔,所以B错误;
故选A.
点评:本题考查了有机物分子式的确定、混合物组成的计算,题目难度不大,注意掌握有机物分子式的确定方法,明确质量守恒及平均分子式在计算中的应用.

练习册系列答案
相关题目
部分弱酸的电离常数如下表:
则下列有关说法正确的是( )
| 弱酸 | HF | HClO | H2CO3 |
| 电离常数 25℃ | 3.53×10-4 | 2.95×10-8 | K1=4.4×10-7 K2=4.7×10-11 |
| A、2ClO-+H2O+CO2=2HClO+CO22- |
| B、等物质的量浓度的 NaHCO3 和 NaClO 的混合溶液中,c(HCO3-)<c(ClO-) |
| C、等物质的量浓度的 NaHCO3 溶液和 Na2CO3 溶液中离子数目一定不相同 |
| D、等物质的量浓度的 NaF 和 NaClO 溶液中所含离子总浓度前者大于后者 |
下列叙述中不正确的是( )
| A、在水溶液里或熔融状态下能够导电的化合物叫做电解质 |
| B、胶体区别于其它分散系的本质特征是分散质的微粒直径在10-9 m-10-7m之间 |
| C、交叉分类法和树状分类法是化学上常用的两种分类方法 |
| D、溶液是电中性的,胶体是带电的 |
下列离子方程式正确的是( )
| A、碳酸钙与醋酸:CaCO3+2H+=Ca2++CO2↑+H2O |
| B、澄清石灰水中加入盐酸:Ca(OH)2+2H+=Ca2++2H2O |
| C、铁片加入稀硫酸中:Fe+2H+=Fe3++H2↑ |
| D、小苏打溶液和醋酸混合:HCO3-+CH3COOH=CH3COO-+CO2↑+H2O |
常温下,发生下列几种反应:①16H++10Z-?+2XO
═2X2++5Z2+8H2O ②2A2++B2═2A3++2B- ③2B-?+Z2═B2+2Z-?根据上述反应,判断下列结论错误的是( )
- 4 |
A、X2+是XO
| ||
B、氧化性强弱的顺序为:XO
| ||
| C、Z2在①③反应中均为还原剂 | ||
| D、溶液中可发生:Z2+2A2+═2A3++2Z? |
下列配制的溶液浓度偏高的是( )
| A、配制盐酸溶液用量筒量取盐酸时,俯视刻度线 |
| B、配制盐酸溶液定容时,仰视容量瓶刻度线 |
| C、称量11.7gNaCl配制0.2mol?L-1NaCL溶液1 000mL时,砝码错放左盘 |
| D、NaOH溶解后未经冷却即注入容量瓶定容至刻度线 |
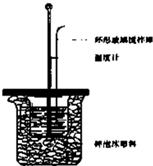 50mL 1.0mol?L-1盐酸跟50mL 1.1mol?L-1氢氧化钠溶液在如图装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热.试回答下列问题:
50mL 1.0mol?L-1盐酸跟50mL 1.1mol?L-1氢氧化钠溶液在如图装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热.试回答下列问题: