题目内容
6.(1)写出下列物质的电子式:HClO
(2)用电子式表示下列物质的形成过程:CaCl2
 .
.
分析 (1)HClO为共价化合物,分子中存在1个氧氢键和1个Cl-O键;
(2)氯化钙是离子化合物,其阴离子写出电荷及电性并用“[]”括起来,阳离子写出电荷和电性即可,离子都满足8电子稳定结构,并用箭头表示电子转移.
解答 解:(1)HClO为共价化合物,分子中存在1个氧氢键和1个Cl-O键,次氯酸的电子式为: ,故答案为:
,故答案为: ;
;
(2)氯化钙为离子化合物,用电子式表示下列物质的形成过程为 ,故答案为:
,故答案为: .
.
点评 本题考查了用电子式书写化合物的性质过程,明确化合物中存在的化学键是解本题关键,难点是用电子式表示化合物的形成过程,注意把握书写方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.下列说法可以证明反应N2(g)+3H2(g)?2NH3(g)已达到平衡状态的是( )
| A. | 1个N≡N键断裂的同时,有3个H-H键形成 | |
| B. | 1个N≡N键断裂的同时,有3个H-H键断裂 | |
| C. | N2、H2、NH3的分子数之比为1:3:2 | |
| D. | 1个N≡N键断裂的同时,有6个H-N键形成 |
17.用化学用语表达下列微粒,错误的是( )
| A. | 氟离子的结构示意图: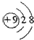 | |
| B. | 氮分子的电子式: | |
| C. | 水分子的电子式:H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$]2-H+ | |
| D. | C-14原子:${\;}_{6}^{14}$C |
14.在2L密闭容器中,盛有2mol X和2molY物质进行如下反应:X(s)+3Y(g)?Z(g),当反应进行到10s后,测得生成0.5mol Z,这期间的平均反应速率为( )
| A. | v(X)=0.5mol•s-1 | B. | v(X)=0.025mol•L-1•s-1 | ||
| C. | v(y)=0.05mol•L-1•s-1 | D. | v(y)=0.075mol•L-1•s-1 |
11.将纯锌片和纯铜片按如图所示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )

| A. | 甲烧杯中锌片逐渐溶解,乙烧杯中锌片不溶解 | |
| B. | 两烧杯中铜片表面均无气泡产生 | |
| C. | 两烧杯中溶液的酸性均减弱 | |
| D. | 甲烧杯中铜片上的电极反应为:Cu2++2e-=Cu |
15.我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛的氧化,其反应如下:HCHO+O2$\stackrel{催化剂}{→}$CO2+H2O.下列有关说法正确的是( )
| A. | 该反应为放热反应 | B. | CO2分子中的化学键为非极性键 | ||
| C. | HCHO分子中只含δ键不含π键 | D. | 设生成1.8gH2O消耗2.24L O2 |
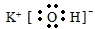 ②C(CH3)4的系统命名:2,2-二甲基丙烷.
②C(CH3)4的系统命名:2,2-二甲基丙烷. 甲醇燃料电池被认为是21世纪电动汽车最佳候选动力源.
甲醇燃料电池被认为是21世纪电动汽车最佳候选动力源.