题目内容
5.A、B、C表示三种短周期元素,它们的原子序数依次增大.A元素原子的最外层电子数是次外层电子数的2倍,B和C可形成BC4型化合物.(1)写出三种元素的元素符号:AC,BSi,CCl.
(2)A、B、C最高价氧化物对应的水化物中,酸性最弱的是:HClO4.
(3)用离子方程式表示用B的氧化物制得B的氧化物对应水化物的原理SiO2+2OH-=SiO32-+H2O;SiO32-+H+=H2SiO3↓.
分析 A元素原子的最外层电子数是次外层电子数的2倍,应为C元素,B和C可形成BC4型化合物,则B为+4价,结合原子序数关系可知B为Si,则C为Cl,以此解答该题.
解答 解:A元素原子的最外层电子数是次外层电子数的2倍,应为C元素,B和C可形成BC4型化合物,则B为+4价,结合原子序数关系可知B为Si,则C为Cl,
(1)由以上分析可知A为C,B为Si,C为Cl,故答案为:C;Si;Cl;
(2)非金属性Cl>C>Si,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,则酸性最弱的是HClO4,故答案为:HClO4;
(3)B为Si,制备硅酸,可由二氧化硅与氢氧化钠溶液反应,然后再与盐酸反应,可生成硅酸,离子方程式为SiO2+2OH-=SiO32-+H2O、SiO32-+H+=H2SiO3↓,
故答案为:SiO2+2OH-=SiO32-+H2O;SiO32-+H+=H2SiO3↓.
点评 本题考查结构性质位置关系应用,为高考常见题型,题目侧重考查原子结构和元素的单质、化合物的性质,元素的推断是解答本题的关键,注意对元素周期律的理解.

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
16.有效氯含量是含氯消毒剂的一个重要指标,其定义为:从HI中氧化出相同量的I2所需Cl2质量与指定含氯消毒剂的质量比.则ClO2的有效氯含量为( )
| A. | 0.263 | B. | 2.63 | C. | 0.132 | D. | 1.32 |
20.实验室中,能用启普发生器制取的是( )
①H2S;
②Cl2;
③HCl;
④H2;
⑤O2;
⑥CO2;
⑦SO2.
①H2S;
②Cl2;
③HCl;
④H2;
⑤O2;
⑥CO2;
⑦SO2.
| A. | 只有①④ | B. | ①④⑥ | C. | ①④⑥⑦ | D. | ③⑥⑦ |
10.下列说法正确的是( )
| A. | 实验中要配制490mL 0.2mol/L KCl溶液,需要托盘天平称量7.3g KCl固体 | |
| B. | 室温下,浓度均为0.1mol/L Na2S2O3和H2SO4溶液,分别取6mL与10mL混合、10mL与10mL混合,可验证Na2S2O3浓度对反应速率的影响 | |
| C. | 往盛有少量淀粉溶液的试管中加入一定量稀硫酸,加热3~4分钟后,再加入NaOH溶液至碱性,最后加入银氨溶液并水浴加热,有银镜产生 | |
| D. | 在中和热的测定实验中,将KOH溶液迅速倒入装有盐酸的量热计中,立即读出并记录溶液的起始温度,充分反应后再读出并记录反应体系的最高温度 |
17.核磁共振氢谱是测定有机物分子结构最有用的工具之一?在有机物分子中,不同的氢原子在质子核磁共振谱中给出的峰值(信号)不同,根据峰(信号)可以确定有机物分子中氢原子的种类?下列有机物分子中,在质子核磁共振谱中只给出一种峰(信号)的是( )
| A. | CH3OH | B. | CH3OCOOCH3 | C. | CH3CH2C(CH3)3 | D. | CH3COOH |
15.下列说法正确的是( )
| A. | 甲苯的一氯取代物有三种同分异构体,它们的熔沸点各不相同 | |
| B. | CH2O2和C2H4O2分子组成上相差一个CH2,所以互为同系物 | |
| C. | 乙醛分别与O2,银氨溶液,新制氢氧化铜反应,均体现了乙醛的还原性 | |
| D. | 淀粉,纤维素,蛋白质都属于天然高分子化合物,可作为人体的供能物质 |
 已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定相似性.
已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定相似性.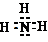 ;C气体的化学式是SO2.
;C气体的化学式是SO2.