题目内容
12.反应3ClO-+2Fe3++10OH-═2FeO42-+5H2O+3Cl-,下列有关该反应的说法中正确的是( )| A. | ClO-作还原剂 | |
| B. | FeO42-为还原产物 | |
| C. | 每产生1 mol FeO42-,转移3 mol电子 | |
| D. | OH-作氧化剂 |
分析 3ClO-+2Fe3++10OH-═2FeO42-+5H2O+3Cl-中,Cl元素的化合价由+1价降低为-1价,Fe元素的化合价由+3价升高为+6价,以此来解答.
解答 解:A.Cl元素的化合价降低,则ClO-作氧化剂,故A错误;
B.Fe失去电子被氧化,则FeO42-为氧化产物,故B错误;
C.每产生1 mol FeO42-,转移1mol×(6-3)=3 mol电子,故C正确;
D.O、H元素的化合价不变,则OH-为反应物,不作氧化剂、还原剂,故D错误;
故选C.
点评 本题考查了氧化还原反应,为高频考点,把握反应中元素化合价变化是解答本题关键,侧重分析与应用能力的考查,注意氧化还原反应中的基本概念,题目难度不大.

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
2.下列关于铵盐的表述正确的是( )
| A. | NH4Cl和NaCl的固体混合物可用升华法分离 | |
| B. | 所有铵盐都易溶于水,所有铵盐中的氮均呈-3价 | |
| C. | 硝铵中不含铵根离子 | |
| D. | 铵态氮肥不能与碱性物质如草木灰混合施用 |
7.有下列8种物质,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )
①甲烷 ②苯 ③聚乙烯 ④1,3-丁二烯 ⑤2-丁炔 ⑥邻二甲苯 ⑦乙醛 ⑧环己烯.
①甲烷 ②苯 ③聚乙烯 ④1,3-丁二烯 ⑤2-丁炔 ⑥邻二甲苯 ⑦乙醛 ⑧环己烯.
| A. | ③④⑤⑧ | B. | ④⑤⑧ | C. | ④⑤⑦⑧ | D. | ③④⑤⑦⑧ |
17.常温下,NCl3是一种淡黄色的油状液体.下列对NCl3的有关叙述不正确的是( )
| A. | NCl3分子是由极性键构成的极性分子 | |
| B. | NCl3分子的空间构型为三角锥形 | |
| C. | NCl3中的所有原子均达到8电子稳定结构 | |
| D. | NF3的沸点比NCl3的沸点低是因为N-F比N-Cl键键能小 |
4.下列关于电解质溶液的正确判断是( )
| A. | 在由水电离产生的C(OH-)=1×10-12 mol•L-1的溶液中,K+、Al3+、SO42-、Cl-一定可以大量共存 | |
| B. | 由0.1 mol/L一元碱BOH溶液的pH=10,可推知BCl溶液呈酸性 | |
| C. | 在pH=0的溶液中,K+、Fe2+、Cl-、NO3-可以大量共存 | |
| D. | 含碳酸氢钠的溶液:K+、SO42-、Cl-、H+能大量共存 |
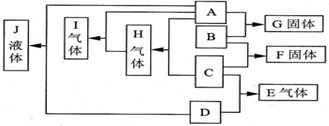
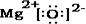 ,其化学键的类型为离子键.
,其化学键的类型为离子键.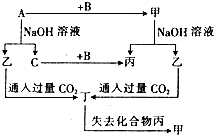 由短周期元素组成的单质A、B、C和四种化合物甲、乙、丙、丁有如图所示的转化关系,已知C是密度最小的气体,甲是电解质.根据图示转化关系回答问题:
由短周期元素组成的单质A、B、C和四种化合物甲、乙、丙、丁有如图所示的转化关系,已知C是密度最小的气体,甲是电解质.根据图示转化关系回答问题: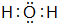 .
.