题目内容
20.将70 g过氧化钠和氧化钠的混合物跟98g水充分反应后,所得氢氧化钠溶液的质量分数为50%.计算原混合物中过氧化钠和氧化钠的质量各为多少克?分析 可设出过氧化钠的质量为x,氧化钠的质量为y,利用化学方程式中物质质量比关系求出生成的氢氧化钠的质量及放出的氧气的质量,求出溶液的总质量,列出方程组求解即可.
解答 解:设混合物中含有过氧化钠的质量为x,氧化钠的质量为y,则:
2Na2O2 +2H2O=4NaOH+O2↑
156 160 32
x $\frac{160x}{156}$ $\frac{32x}{156}$
Na2O+H2O=2NaOH
62 80
y $\frac{80y}{62}$
可得方程组:$\left\{\begin{array}{l}{x+y=70}\\{\frac{160x}{156}+\frac{80y}{62}=(70+98-\frac{32x}{156})×50%}\end{array}\right.$,
解得:x=39g、y=31g,
答:过氧化钠的质量为39g,氧化钠的质量为31g.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应的原理为解答关键,注意掌握守恒思想在化学计算中的应用方法,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
10.下列物质互为同分异构体的一组是( )
| A. | 35Cl和37Cl | B. | O2和O3 | ||
| C. | CH3CH2OH和CH3OCH3 | D. | 甲烷和丁烷 |
11.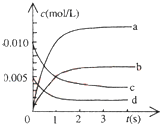 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
(1)写出该反应的平衡常数表达式:K=$\frac{[N{O}_{2}]^{2}}{[NO]^{2}[{O}_{2}]}$.
(2)如图中表示NO2的变化的曲线是b.
(3)能说明该反应已达到平衡状态的是bc.
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆 (NO)=2v正(O2) d.容器内密度保持不变
(4)某同学查阅资料得知,该反应K300℃>K350℃;25℃时,生成1mol NO2,热量变化为56.4kJ.但是该同学由于疏忽,忘记注明“+”、“-”.根据题目信息,该反应的热化学方程式为2NO(g)+O2(g)?2NO2(g)△H=-112.8KJ/mol.
(5)为使该反应的反应速率增大,且平衡向正反应方向移动的是c.
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂.
 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)如图中表示NO2的变化的曲线是b.
(3)能说明该反应已达到平衡状态的是bc.
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆 (NO)=2v正(O2) d.容器内密度保持不变
(4)某同学查阅资料得知,该反应K300℃>K350℃;25℃时,生成1mol NO2,热量变化为56.4kJ.但是该同学由于疏忽,忘记注明“+”、“-”.根据题目信息,该反应的热化学方程式为2NO(g)+O2(g)?2NO2(g)△H=-112.8KJ/mol.
(5)为使该反应的反应速率增大,且平衡向正反应方向移动的是c.
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂.
8.下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是( )
| A. | Cu(OH)2与盐酸 Cu(OH)2与醋酸 | |
| B. | BaCl2溶液与Na2SO4溶液 Ba(OH)2溶液与Na2SO4溶液 | |
| C. | NaHCO3溶液与NaHSO4溶液 Na2CO3溶液与NaHSO4溶液 | |
| D. | 石灰石与硝酸 生石灰与盐酸 |
5.下列有关表述正确的是( )
(1)-OH 与 组成元素相同,含有的电子数也相同
组成元素相同,含有的电子数也相同
(2)HCN分子的结构式:H-C≡N
(3)Fe2+的离子结构示意图:
(4)CO2的分子模型示意图:
(5)丙烷的分子结构模型示意图:
(6)次氯酸的电子式为:
(7)铜绿主要成分的化学式:Cu(OH)2CO3
(8)熔化时NaHSO4的电离方程式为NaHSO4=Na++HSO4-.
(1)-OH 与
 组成元素相同,含有的电子数也相同
组成元素相同,含有的电子数也相同(2)HCN分子的结构式:H-C≡N
(3)Fe2+的离子结构示意图:

(4)CO2的分子模型示意图:

(5)丙烷的分子结构模型示意图:

(6)次氯酸的电子式为:

(7)铜绿主要成分的化学式:Cu(OH)2CO3
(8)熔化时NaHSO4的电离方程式为NaHSO4=Na++HSO4-.
| A. | (1)(2)(4)(6) | B. | (2)(3)(5) | C. | (1)(4)(5)(8) | D. | (1)(2)(5)(8) |
12.下列物质中,含有共价键的离子化合物是( )
| A. | NH3 | B. | H2 | C. | NaOH | D. | H2SO4 |
3.CO2通入下列溶液中,不可能产生沉淀的是( )
| A. | 氯化钙溶液 | B. | 澄清石灰水 | C. | 饱和碳酸钠溶液 | D. | 次氯酸钙溶液 |
