题目内容
下列实验中所选用的仪器或实验基本操作合理的是
①用50 mL量筒量取5.2 mL稀硫酸 ②用酒精洗涤粘有硫粉的试管 ③用托盘天平称量10.1g氯化钠晶体 ④实验中不慎将手指划破,可立即用FeCl3溶液止血 ⑤用瓷坩埚熔融NaOH ⑥用饱和NaHCO3溶液除去CO2中的少量SO2
A.①②③④ B.③④⑥ C.③④⑤ D.③⑤⑥
B
【解析】
试题分析:①量取5.2 mL稀硫酸应用10mL量筒;②用酒精洗涤粘有硫粉的试管应先用二硫化碳洗涤再用水洗;③用托盘天平称量10.1g氯化钠晶体,合理;④实验中不慎将手指划破,可立即用FeCl3溶液止血,利用胶体遇电解质溶液发生聚沉,合理;⑤陶瓷的成分二氧化硅高温下与氢氧化钠反应,不能用瓷坩埚熔融NaOH ;⑥用饱和NaHCO3溶液除去CO2中的少量SO2,合理,综上所述选B。
考点:考查化学实验基本操作。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
t ℃时,在体积不变的密闭容器中发生反应:X(g)+3Y(g)  2Z(g),各组分在不同时刻的浓度如下表,下列说法正确的是:
2Z(g),各组分在不同时刻的浓度如下表,下列说法正确的是:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
2 min末浓度/mol·L-1 | 0.08 | a | b |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
A.平衡时,X的转化率为20%
B.t ℃时,该反应的平衡常数为40
C.增大平衡后的体系压强, v正增大,v逆减小,平衡向正反应方向移动
D.前2 min内,用Y的变化量表示的平均反应速率v(Y) = 0.03 mol·L-1·min-1
 已知草酸为二元弱酸:
已知草酸为二元弱酸:H2C2O4?HC2O4-+H+ Ka1
HC2O4-?C2O42-+H+ Ka2
常温下,向某浓度的草酸溶液中逐滴加入一定量浓度的KOH溶液,所得溶液中H2C2O4、HC2O4-、C2O42-三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法中不正确的是
( )
| A、pH=1.2溶液中:c(K+)+c(H+)=c(OH-)+c(H2C2O4) |
| B、pH=2.7溶液中:c2(HC2O4-)/[c(H2C2O4)×c(C2O42-)]=1000 |
| C、将相同物质的量KHC2O4和K2C2O4固体完全溶于水可配得pH为4.2的混合液 |
| D、向pH=1.2的溶液中加KOH溶液将pH增大至4.2的过程中水的电离度一直增大 |
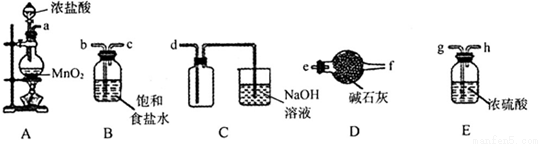
下列实验操作不能达到预期目的是( )
A、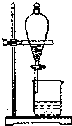 分离CH3COOC2H5和饱和碳酸钠溶液 |
B、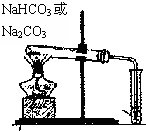 鉴别碳酸钠和碳酸氢钠 |
C、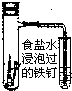 铁的吸氧腐蚀实验 |
D、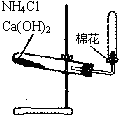 实验室制备氨气 |

 Cu+FeS+ SO2 ,FeS+2HCl
Cu+FeS+ SO2 ,FeS+2HCl FeCl2+H2S。
FeCl2+H2S。
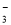 、AlO
、AlO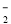 、K+、S2-等离子
、K+、S2-等离子