题目内容
9.用相同体积的 0.1mol/L的BaCl2溶液,能分别使相同体积的Fe2(SO4)3、ZnSO4和Na2SO4三种溶液中的SO42-完全转化为BaSO4沉淀,则三种溶液的物质的量浓度之比为( )| A. | 3:2:1 | B. | 1:2:3 | C. | 3:1:1 | D. | 1:3:3 |
分析 等体积等物质的量浓度的BaCl2溶液含有BaCl2的物质的量相同,由Ba2++SO42-=BaSO4↓可知生成BaSO4物质的量相同,设BaSO4的物质的量为3mol,计算Fe2(SO4)3、ZnSO4、Na2SO4的物质的量,因三种溶液的体积相同,则物质的量之比等于其浓度之比.
解答 解:等体积等物质的量浓度的BaCl2溶液含有BaCl2的物质的量相同,由Ba2++SO42-=BaSO4↓可知生成BaSO4物质的量相同,设BaSO4的物质的量为3mol,
则:n[Fe2(SO4)3]=$\frac{1}{3}$n(BaSO4)=$\frac{1}{3}$×3mol=1mol,
n(ZnSO4)=n(BaSO4)=3mol,
n(K2SO4)=n(BaSO4)=3mol,
三种溶液的体积相同,物质的量浓度之比等于物质的量之比,
所以相同体积的Fe2(SO4)3、ZnSO4、K2SO4溶液的物质的量浓度之比为1mol:3mol:3molmol=1:3:3,
故选D.
点评 本题考查溶液中离子浓度的计算,属于无数据型计算,题目难度中等,根据消耗氯化钡相等确定各物质的物质的量是解答关键,注意掌握物质的量浓度的概念及表达式,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
19.150mL 1mol/L 的氢氧化钠溶液吸收了 2.24L 标准状况下的二氧化碳后,对于溶液中各离子的关系,下列说法错误的是( )
| A. | HCO3-个数多于CO32-个数 | |
| B. | 逐滴加入稀盐酸,刚开始会产生气体 | |
| C. | c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) | |
| D. | 2c(Na+)=3[c(HCO3-)+c(CO32-)+c(H2CO3)] |
20.根据如图,判断下列说法中错误的是( )
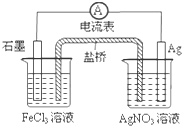

| A. | 导线上电子由Ag极流向石墨极 | B. | 负极电极反应式:Fe3++e-═Fe2+ | ||
| C. | 盐桥中阴离子移向AgNO3溶液 | D. | 总反应为:Fe3++Ag═Fe2++Ag+ |
17.下列电解质溶液的有关叙述正确的是( )
| A. | 在CH3COONa溶液中加入适量CH3COOH,可使c(Na+)=c(CH3COO-) | |
| B. | 在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大 | |
| C. | 含1 mol KOH的溶液与1 mol CO2完全反应后,溶液中c(K+)=c(HCO${\;}_{3}^{-}$) | |
| D. | 同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7 |
4.下列状态的物质,既能导电又属于电解质的是( )
| A. | 熔融的KOH | B. | NaCl溶液 | C. | 液态HCl | D. | MgCl2晶体 |
14.“保护环境,就是保护人类自己.”下列环境问题与产生的主要原因不相符的是( )
①“臭氧空洞”主要是大量使用氟氯代烃等引起的
②“光化学烟雾”主要是由NO2等引起的
③“酸雨”主要是由空气中CO2浓度增大引起的
④“白色污染”主要是由聚乙烯塑料等引起的
⑤“厄尔尼诺”现象是由空气中CO2浓度增大引起的
⑥“温室效应”主要是由空气中CO2浓度增大引起的
⑦“赤潮”主要是由水体中P、N等元素过量引起的.
①“臭氧空洞”主要是大量使用氟氯代烃等引起的
②“光化学烟雾”主要是由NO2等引起的
③“酸雨”主要是由空气中CO2浓度增大引起的
④“白色污染”主要是由聚乙烯塑料等引起的
⑤“厄尔尼诺”现象是由空气中CO2浓度增大引起的
⑥“温室效应”主要是由空气中CO2浓度增大引起的
⑦“赤潮”主要是由水体中P、N等元素过量引起的.
| A. | 只有①② | B. | 只有②③⑤ | C. | 全部 | D. | 只有③ |
1.氧化还原反应与四种基本反应类型反应的关系如图所示,则下列化学反应属于区域3的是( )

| A. | Zn+H2SO4═ZnSO4+H2↑ | B. | 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe | ||
| C. | CaO+H2O═Ca(OH)2 | D. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ |
19.某温度时,N2与H2反应过程中的能量变化如图所示.下列叙述正确的是( )
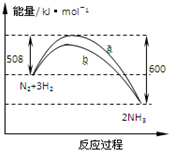

| A. | 1 mo N2与3 mo H2反应可以放出92 kJ的热量 | |
| B. | b曲线是加入催化剂时的能量变化曲线 | |
| C. | 加入催化剂,该反应的焓变减小 | |
| D. | 正反应的活化能等于逆反应的活化能 |