题目内容
下列对化学反应的认识正确的是
| A.化学反应必然引起物质状态的变化 |
| B.化学反应一定有化学键的断裂和生成 |
| C.需要加热的反应一定是吸热反应 |
| D.若反应物的总能量高于生成物的总能量,则该反应是吸热反应 |
B
解析试题分析:化学反应不一定引起物质状态的变化,A不正确;化学反应的实质就是旧键断裂和新键的形成,选项B正确;反应是放热反应还是吸热反应,与反应条件无关系,只与反应物和生成物总能量的相对大小有关系。如果反应物的总能量关于生成物的总能量,反应就是放热反应,反之是吸热反应,CD均不正确,答案选B。
考点:考查化学反应的实质、特征以及反应热的有关判断
点评:该题是基础性试题的考查,试题紧扣教材,针对性强。有利于巩固学生的基础,调动学生的学习兴趣,提高学生的应试能力和学习效率。注意有关知识的积累和总结,难度不大。

以下既有反应热又有溶解热且都是吸热的是
| A.浓硫酸与NaOH溶液 | B.KNO3加入水中 |
| C.NH4NO3加入水中 | D.CaO加入水中 |
下列叙述不正确的是
| A.纯银器表面在空气中因化学腐蚀渐渐变暗 |
| B.氢氧燃料电池是一种将化学能转化为电能的装置 |
| C.可用浸有酸性高锰酸钾溶液的滤纸来检验二氧化硫气体的漂白性 |
| D.塑料袋在全球“失宠”,有偿使用成为风尚,是因为塑料袋填埋占用土地,且难以降解 |
下列说法中正确的是
| A.化学反应中的能量变化,表现形式除热量外还可以是光能和电能等 |
| B.化学反应中的能量变化不一定服从能量守恒定律 |
| C.在一个确定的化学反应关系中,反应物的总能量与生成物的总能量可能相同 |
| D.在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量 |
今有如下三个热化学方程式:
H2(g)+ 1/2 O2(g) = H2O(g) ; △H=a kJ/mol
H2(g)+ 1/2 O2(g) =H2O(l) ; △H=b kJ/mol
2 H2(g)+ O2(g) ="2" H2O(l) ; △H=c kJ/mol
下列关于它们的表述正确的是( )
| A.它们都是吸热反应 | B.a、b和c均为正值 |
| C.反应热的关系:a=b | D.反应热的关系:2b=c |
下列对化学反应的认识错误的是
| A.会引起化学键的变化 | B.会产生新的物质 |
| C.必然引起物质状态的变化 | D.必然伴随着能量的变化 |
下列反应既是氧化还原反应,又是吸热反应的是
| A.Ba(OH)2·8H2O与NH4Cl的反应 |
| B.铝片与稀硫酸反应 |
| C.甲烷在空气中燃烧 |
| D.灼热的焦炭与CO2反应 |
工业上也可以用CO2和H2反应制得甲醇。在2×105Pa、300℃的条件下,若有44g CO2与6g H2恰好完全反应生成气体甲醇和水,放出49.5kJ的热量。试写出该反应的热化学方程式: 。
某次实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如下图所示(实线)。
试回答下列问题: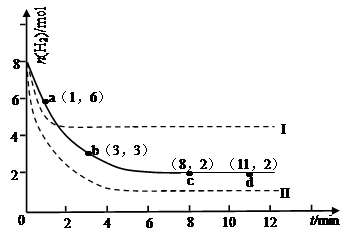
(1)a点正反应速率 (填大于、等于或小于)逆反应速率。
(2)下列时间段平均反应速率最大的是 ,最小的是 。
| A.0~1min |
| B.1~3min |
| C.3~8min |
| D.8~11min |
(4)仅改变某一实验条件再进行两次实验,测得H2的物质的量随时间变化如图中虚线所示,曲线I对应的实验条件改变是 ,曲线II对应的实验条件改变是 。