题目内容
锌粒与50mL稀硫酸反应,10分钟末时反应物均有剩余,收集到标准状况下224mLH2,反应前后溶液体积不变,此时间段内,反应的平均反应速率为( )
| A、v(Zn)=6.5g?min-1 |
| B、v(H2SO4)=0.05mol?L-1?min-1 |
| C、v(SO42-)=0.02mol?L-1?min-1 |
| D、v(H2)=22.4mL?min-1 |
考点:反应速率的定量表示方法
专题:
分析:根据n=
,速率之比等于化学计量数之比及v=
进行计算.
| V |
| Vm |
| △c |
| t |
解答:
解:n(H2)=
=0.01mol,
A.锌粒为固体,不可用于表示化学反应速率,故A错误;
B.n(H2SO4)=n(H2)=0.01mol,故v(H2SO4)=
=0.02mol?L-1?min-1,故B错误;
C.硫酸根离子为参加反应,故硫酸根离子的速率为0,故C错误;
D.v(H2)=
=22.4mL?min-1,故D正确;
故选D.
| 0.224 |
| 22.4 |
A.锌粒为固体,不可用于表示化学反应速率,故A错误;
B.n(H2SO4)=n(H2)=0.01mol,故v(H2SO4)=
| ||
| 10 |
C.硫酸根离子为参加反应,故硫酸根离子的速率为0,故C错误;
D.v(H2)=
| 224 |
| 10 |
故选D.
点评:本题考查化学反应速率的表示方法及相关计算,难度不大.要注意固体不可用于表示化学反应速率.

练习册系列答案
相关题目
在一密闭容器中充入1molH2和1molI2,发生反应:H2(g)+I2(g)?2HI(g)△H<0.下列说法正确的是( )
| A、升高温度,平衡向逆反应方向移动,正反应速率减慢 |
| B、容积不变,加入1molN2(N2不参加反应),反应速率不变 |
| C、压强不变,加入1molN2(N2不参加反应),反应速率不变 |
| D、容积不变,加入1molN2,则正反应速率加快,逆反应速率减慢 |
下列反应不属于取代反应的是( )
| A、CHCl3+HF→CHFCl2+HCl | |||
B、2CH3CH2OH
| |||
| C、H2C=CH2+Br2→CH2Br-CH2Br | |||
D、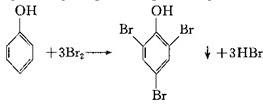 |
温度为T时,向2.0L恒荣密闭容器中充入2.0molNO2,反应2NO2(g)?N2O4(g)经一段时间后达到平衡,反应过程中测定的部分数据见下表:下列说法正确的是( )
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(N2O4)/mol | 0 | 0.12 | 0.18 | 0.20 | 0.20 |
| A、反应在前50s的平均速率为v(NO2)=0.0012mol?L-1?s-1 |
| B、保持温度不变,向平衡后的容器中充入1.0 mol N2O4时,v(正)<v(逆) |
| C、保持其他条件不变,升高温度达到新平衡时K=0.125,则反应的△H<0 |
| D、T温度时,若起始向容器中充入2.0molN2O4,则平衡时N2O4的转化率大于80% |
已知H2S在水溶液中分两步电离:
第一步:H2S?H++HS- K1=
=1.3×10-7;
第二步:HS-?H++S2- K2=
=7.1×10-15.由此可知( )
第一步:H2S?H++HS- K1=
| C(H+)(HS-) |
| C(H2S) |
第二步:HS-?H++S2- K2=
| C(H+)C(S2-) |
| C(HS-) |
| A、H2S是二元弱酸 |
| B、H2S溶液中不存在HS- |
| C、0.1mol?L-1H2S溶液的pH约为4 |
| D、NaHS的电离方程式为NaHS?Na++H++S2- |
铅蓄电池在现代生活中有广泛的应用.其电极材料分别是Pb和PbO2,电解质溶液是硫酸溶液,它的充、放电反应为:Pb(s)+PbO2(s)+2H2SO4(aq)
2PbSO4(s)+2H2O(l),下列说法正确的是( )
| 放电 |
| 充电 |
| A、电池放电时,每消耗0.1molPb,共生成0.1molPbSO4 |
| B、电池放电后,电池中溶液的pH变大 |
| C、电池充电时,阴极反应为:PbSO4(s)+2H2O(l)-2e-═PbO2(s)+4H+(aq)+SO42-(aq) |
| D、电池充电时,把铅蓄电池的正极与外电源负极相连 |
对于锌-铜-稀H2SO4组成的原电池装置中,当导线中有1mol电子通过时,理论上的电极变化是( )
①锌片溶解了32.5g②锌片增重32.5g③铜片上析出了1gH2④铜片上析出1mol H2⑤溶液中的SO42-移向锌极⑥溶液中SO42-移向铜极.
①锌片溶解了32.5g②锌片增重32.5g③铜片上析出了1gH2④铜片上析出1mol H2⑤溶液中的SO42-移向锌极⑥溶液中SO42-移向铜极.
| A、①③⑤ | B、①④⑥ |
| C、②③⑤ | D、②④⑥ |
下列化学用语表述正确的是( )
A、“84消毒液”中有效成分NaCIO的电子式:Na+[
| ||||||||||||||
B、食盐中阴离子的核外电子排布式: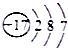 | ||||||||||||||
C、聚丙烯的结构简式: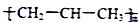 | ||||||||||||||
| D、乙烯的结构简式:CH2CH2 |
 如图所示将2mol SO2和1mol O2混合置于体积可变的等压容器中,在一定温度下发生如下反应:2SO2(g)+O2(g)?2SO3(g);△H<0.该反应达到平衡状态A时,测得气体总物质的量为2.4mol.若SO2、O2、SO3的起始物质的量分别用a、b、c 表示,回答下列问题:
如图所示将2mol SO2和1mol O2混合置于体积可变的等压容器中,在一定温度下发生如下反应:2SO2(g)+O2(g)?2SO3(g);△H<0.该反应达到平衡状态A时,测得气体总物质的量为2.4mol.若SO2、O2、SO3的起始物质的量分别用a、b、c 表示,回答下列问题: