题目内容
阿伏加德罗常数约为6.02×1023mol-1,下列说法中一定正确的是( )
| A、常温常压下,22g氧气和26g臭氧混合气体所含氧原子总数为3×6.02×1023 |
| B、1L0.5mol/L的CH3COONa溶液中含有的CH3COO-数为0.5×6.02×1023 |
| C、常温常压下,16g14CH4所含中子数为8×6.02×1023 |
| D、1molCl2发生反应时,转移的电子数一定是2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、依据氧元素守恒计算;
B、醋酸钠溶液中醋酸根离子水解;
C、依据n=
计算物质的量结合质子数+中子数=质量数;
D、1mol氯气自身氧化还原反应电子转移1mol,只做氧化剂电子转移2mol.
B、醋酸钠溶液中醋酸根离子水解;
C、依据n=
| m |
| M |
D、1mol氯气自身氧化还原反应电子转移1mol,只做氧化剂电子转移2mol.
解答:
解:A、依据氧元素守恒计算,22g氧气和26g臭氧混合气体所含氧原子总数=
×NA=3×6.02×1023,故A正确;
B、醋酸钠溶液中醋酸根离子水解,1L0.5mol/L的CH3COONa溶液中含有的CH3COO-数小于0.5×6.02×1023,故B错误;
C、依据n=
计算物质的量=
,结合质子数+中子数=质量数,所含中子数=
×(14-6+0)×NA=
×8×6.02×1023,故C错误;
D、1mol氯气自身氧化还原反应电子转移1mol,只做氧化剂电子转移2mol,故D错误;
故选A.
| 48g |
| 16g/mol |
B、醋酸钠溶液中醋酸根离子水解,1L0.5mol/L的CH3COONa溶液中含有的CH3COO-数小于0.5×6.02×1023,故B错误;
C、依据n=
| m |
| M |
| 16g |
| 18g/mol |
| 16 |
| 18 |
| 16 |
| 18 |
D、1mol氯气自身氧化还原反应电子转移1mol,只做氧化剂电子转移2mol,故D错误;
故选A.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积条件应用,氧化还原反应电子转移计算,掌握基础是关键,题目较简单.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
已知:CH4(g)+2O2(g)→CO2(g)+2H2O(l)+890kJ、CO(g)+
O2(g)→CO2(g)+282.5kJ.标准情况下,由CH4、CO、CO2组成的混合气体89.6L完全燃烧时能放出1010kJ的热量,并生成18g液体水,则燃烧前混合气体中CO占的体积分数为( )
| 1 |
| 2 |
| A、50% | B、60% |
| C、70% | D、80% |
下列表达方式正确的是( )
A、碳-12原子
| ||
B、羟基电子式 | ||
C、硫离子结构示意图 | ||
D、CH4S的结构式 |
下列水解离子方程式正确的是( )
| A、CH3COO-+H2O?CH3COOH+OH- |
| B、NH4++H2O?NH4OH+H+ |
| C、Fe3++H2O?Fe(OH)3+H+ |
| D、Al3++3HCO3-═Al(OH)3↓+3CO2↑ |
下列物质为纯净物的是( )
| A、冰醋酸 | B、医用酒精 |
| C、福尔马林 | D、汽油 |

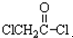 与足量的NaOH溶液共热充分反应的化学方程式:
与足量的NaOH溶液共热充分反应的化学方程式: