题目内容
按要求写出下列方程式
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ.则表示甲醇燃烧热的热化学方程式是:
(2)已知在25℃、101kPa时,CO的燃烧热为283kJ/mol,相同条件下,若2molCH4完全燃烧生成液态水,所放出的热量为1molCO完全燃烧放出热量的6.3倍,CH4完全燃烧反应的热化学方程式是:
(3)Al(OH)3的电离反应方程式:
(4)H2S的电离反应方程式:
(5)NaHSO4溶于水的电离方程式 .
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ.则表示甲醇燃烧热的热化学方程式是:
(2)已知在25℃、101kPa时,CO的燃烧热为283kJ/mol,相同条件下,若2molCH4完全燃烧生成液态水,所放出的热量为1molCO完全燃烧放出热量的6.3倍,CH4完全燃烧反应的热化学方程式是:
(3)Al(OH)3的电离反应方程式:
(4)H2S的电离反应方程式:
(5)NaHSO4溶于水的电离方程式
考点:热化学方程式,电离方程式的书写
专题:
分析:(1)燃烧热是1mol可燃物完全燃烧生成稳定氧化物时放出的热量;在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ,32g甲醇燃烧生成CO2和液态水时放热22.68kJ×32=725.76kJ,1mol甲醇质量为32克,所以完全燃烧1mol甲醇生成二氧化碳和液态水放热725.76KJ;
(2)根据CO的燃烧热计算,2molCH4完全燃烧生成液态水,所放出的热量,再根据热化学方程式的书写原则进行书写;
(3)Al(OH)3分酸式、碱式电离;
(4)H2S分两步电离;
(5)NaHSO4是强酸的酸式盐,完全电离.
(2)根据CO的燃烧热计算,2molCH4完全燃烧生成液态水,所放出的热量,再根据热化学方程式的书写原则进行书写;
(3)Al(OH)3分酸式、碱式电离;
(4)H2S分两步电离;
(5)NaHSO4是强酸的酸式盐,完全电离.
解答:
解:(1)1mol甲醇完全燃烧生成二氧化碳和液态水放热725.8KJ;燃烧热的热化学方程式为:CH3OH(l)+
O2(g)═CO2(g)+2H2O(l)△H=-725.76 kJ?mol-1,
故答案为:CH3OH(l)+
O2(g)═CO2(g)+2H2O(l)△H=-725.76 kJ?mol-1;
(2)CO的燃烧热为283kJ/mol.相同条件下,2molCH4完全燃烧生成液态水,所放出的热量为283kJ×6.3=1782.9kJ,故甲烷完全燃烧生成液态水的热化学方程式为:CH4(g)+2O2 (g)=CO2(g)+2H2O(1)△H=-891kJ/mol,
故答案为:CH4(g)+2O2 (g)=CO2(g)+2H2O(1)△H=-891kJ/mol;
(3)Al(OH)3分酸式、碱式电离,H++AlO2-+H2O?Al(OH)3?Al3++3OH-;
故答案为:H++AlO2-+H2O?Al(OH)3?Al3++3OH-;
(4)H2S分两步电离,H2S?H++HS-、HS-?H++S2-,故答案为:H2S?H++HS-、HS-?H++S2-;
(5)NaHSO4是强酸的酸式盐,完全电离,NaHSO4=Na++H++SO42-,故答案为:NaHSO4=Na++H++SO42-.
| 3 |
| 2 |
故答案为:CH3OH(l)+
| 3 |
| 2 |
(2)CO的燃烧热为283kJ/mol.相同条件下,2molCH4完全燃烧生成液态水,所放出的热量为283kJ×6.3=1782.9kJ,故甲烷完全燃烧生成液态水的热化学方程式为:CH4(g)+2O2 (g)=CO2(g)+2H2O(1)△H=-891kJ/mol,
故答案为:CH4(g)+2O2 (g)=CO2(g)+2H2O(1)△H=-891kJ/mol;
(3)Al(OH)3分酸式、碱式电离,H++AlO2-+H2O?Al(OH)3?Al3++3OH-;
故答案为:H++AlO2-+H2O?Al(OH)3?Al3++3OH-;
(4)H2S分两步电离,H2S?H++HS-、HS-?H++S2-,故答案为:H2S?H++HS-、HS-?H++S2-;
(5)NaHSO4是强酸的酸式盐,完全电离,NaHSO4=Na++H++SO42-,故答案为:NaHSO4=Na++H++SO42-.
点评:本题考查了热化学方程式、水解方程式的书写、电离方程式的书写,题目难度中等,注意掌握热化学方程式、水解方程式.

练习册系列答案
相关题目
下列有机物命名正确的是( )
A、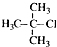 2-甲基-2-氯丙烷 |
B、 1,3,4-三甲苯 |
C、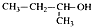 2-甲基-1-丙醇 |
D、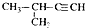 2-甲基-3-丁炔 |
一定温度下,向0.1mol/LNaC1O溶液中分别加入少量下列固体(忽略溶液体积变化),可使c(C1O-)增大的是( )
| A、NaOH |
| B、NH4NO3 |
| C、Na2SO3 |
| D、FeC12 |
下列事实不能说明亚硝酸是弱电解质的是( )
| A、NaNO2溶液的pH大于7 |
| B、向HNO2溶液中加入NaNO2固体,溶液的PH变大 |
| C、常温下0.1mol/LHNO2溶液的pH为2.1 |
| D、用HNO2溶液作导电试验,灯泡很暗 |
为了验证NaHCO3固体中是否含有Na2CO3,下列实验及判断中,正确的是( )
| A、加热,观察是否有气体放出 |
| B、溶于水后加BaC12,看有无沉淀 |
| C、溶于水后加石灰水,看有无沉淀 |
| D、取固体变色试样加盐酸,看是否有气泡产生 |
对于弱电解质的稀溶液,温度一定时,加水稀释至原来浓度的1/n时,其电离度将增大到原溶液电离度的
倍,现有pH=2的某一元弱酸溶液10mL,加水稀释至1L后,溶液的pH( )
| n |
| A、等于4 | B、在3~4之间 |
| C、等于3 | D、在2~3之间 |
阿伏加德罗常数约为6.02×1023mol-1,下列说法中一定正确的是( )
| A、常温常压下,22g氧气和26g臭氧混合气体所含氧原子总数为3×6.02×1023 |
| B、1L0.5mol/L的CH3COONa溶液中含有的CH3COO-数为0.5×6.02×1023 |
| C、常温常压下,16g14CH4所含中子数为8×6.02×1023 |
| D、1molCl2发生反应时,转移的电子数一定是2NA |