题目内容
11.实验室用浓盐酸制备Cl2时,制备的Cl2中往往含有HCl气体,下列说法正确的为( )| A. | 可以用湿润的蓝色石蕊试纸检验Cl2中的HCl | |
| B. | 可以用湿润的有色布条检验Cl2中的HCl | |
| C. | 可以用饱和NaCl溶液除去Cl2中的HCl | |
| D. | 可以用饱和NaOH溶液除去Cl2中的HCl |
分析 制备的Cl2中往往含有HCl气体,利用饱和食盐水可除杂,HCl极易溶于水,食盐水抑制氯气的溶解,氯气与水反应生成HClO具有漂白性,以此来解答.
解答 解:A.氯气与水反应生成HClO,具有漂白性,不能用湿润的蓝色石蕊试纸检验,故A不选;
B.氯气与水反应生成HClO,具有漂白性,不能用湿润的有色布条检验,故B不选;
C.HCl极易溶于水,食盐水抑制氯气的溶解,则食盐水可除杂,故C选;
D.二者均与NaOH反应,不能除杂,故D不选;
故选C.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、混合物分离、物质检验为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.下列离子方程式中,书写正确的是( )
| A. | 醋酸与烧碱混合:H++OH-═H2O | |
| B. | 大理石中加入盐酸:CO32-+2H+═CO2↑+H2O | |
| C. | 稀硫酸滴在铁片上:Fe+2H+═Fe2++H2↑ | |
| D. | 硫酸铜溶液和氢氧化钡溶液混合:Cu2++2OH-═Cu(OH)2↓ |
19.下列各组中属于同位素关系的是( )
| A. | ${\;}_{3}^{6}$Li与${\;}_{3}^{7}$Li | B. | D2O与H2O | ||
| C. | ${\;}_{6}^{14}$C与${\;}_{7}^{14}$N | D. | 金刚石与石墨 |
6.某有机物X能发生水解反应,水解产物为Y和Z.同温同压下,相同质量的Y和Z的蒸气所占体积相同,化合物X可能是( )
| A. | 甲酸乙酯 | B. | 乙酸甲酯 | C. | 麦芽糖 | D. | 蔗糖 |
16.下列 ①0.5mol CH4; ②标况下11.2LH2; ③4℃时的9mL水; ④0.2molNa3PO4所含原子数目按由大到小顺序排列的是( )
| A. | ①④②③ | B. | ④③②① | C. | ②③④① | D. | ①④③② |
3.下列物质的主要成分属于天然纤维素的是( )
| A. | 聚乙烯 | B. | 天然橡胶 | C. | 棉花 | D. | 涤纶 |
1. 6种相邻短周期主族元素的相对位置如下表,M元素原子核外电子数是Y元素原子核外电子数的2倍,W元素原子的次外层电子数是最外层电子数的2倍.用化学用语回答下列问题:
6种相邻短周期主族元素的相对位置如下表,M元素原子核外电子数是Y元素原子核外电子数的2倍,W元素原子的次外层电子数是最外层电子数的2倍.用化学用语回答下列问题:
(1)Y在周期表中的位置是第二周期第VIA族.
(2)X、Y、Z三种元素的原子半径由大到小的顺序是r(N)>r(O)>r(F).
(3)W、M、Q三种元素最高价氧化物对应的水化物中,酸性由强到弱的顺序是HClO4>H2SO4>H2SiO3.
(4)W的最高价氧化物可以和Z的氢化物反应,利用该反应可刻蚀玻璃,反应的化学方程式是SiO2+4HF═SiF4+2H2O.
(5)X的含10个电子的气态氢化物甲是一种重要的化工原料.甲的电子式是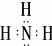 ,实验室制备甲的化学方程式是2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,甲可以与X的最高价氧化物对应的水化物溶液反应生成盐乙,乙溶液中的离子浓度由大到小的顺序是c(NO3-)>c(NH4+)>c(H+)>c(OH-).X的含18个电子的气态氢化物丙可与空气构成一种环保型碱性燃料电池,电池工作时丙发生的电极反应方程式是N2H4-4e-+4OH-═N2+4H2O.
,实验室制备甲的化学方程式是2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,甲可以与X的最高价氧化物对应的水化物溶液反应生成盐乙,乙溶液中的离子浓度由大到小的顺序是c(NO3-)>c(NH4+)>c(H+)>c(OH-).X的含18个电子的气态氢化物丙可与空气构成一种环保型碱性燃料电池,电池工作时丙发生的电极反应方程式是N2H4-4e-+4OH-═N2+4H2O.
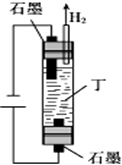
(6)工业上用如图所示装置电 解Q元素的钠盐溶液丁,获得一种含Q元素的消毒剂.该反应的离子方程式是Cl-+H2O═ClO-+H2↑.
 6种相邻短周期主族元素的相对位置如下表,M元素原子核外电子数是Y元素原子核外电子数的2倍,W元素原子的次外层电子数是最外层电子数的2倍.用化学用语回答下列问题:
6种相邻短周期主族元素的相对位置如下表,M元素原子核外电子数是Y元素原子核外电子数的2倍,W元素原子的次外层电子数是最外层电子数的2倍.用化学用语回答下列问题:| X | Y | Z | |
| W | M | Q |
(2)X、Y、Z三种元素的原子半径由大到小的顺序是r(N)>r(O)>r(F).
(3)W、M、Q三种元素最高价氧化物对应的水化物中,酸性由强到弱的顺序是HClO4>H2SO4>H2SiO3.
(4)W的最高价氧化物可以和Z的氢化物反应,利用该反应可刻蚀玻璃,反应的化学方程式是SiO2+4HF═SiF4+2H2O.
(5)X的含10个电子的气态氢化物甲是一种重要的化工原料.甲的电子式是
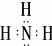 ,实验室制备甲的化学方程式是2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,甲可以与X的最高价氧化物对应的水化物溶液反应生成盐乙,乙溶液中的离子浓度由大到小的顺序是c(NO3-)>c(NH4+)>c(H+)>c(OH-).X的含18个电子的气态氢化物丙可与空气构成一种环保型碱性燃料电池,电池工作时丙发生的电极反应方程式是N2H4-4e-+4OH-═N2+4H2O.
,实验室制备甲的化学方程式是2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,甲可以与X的最高价氧化物对应的水化物溶液反应生成盐乙,乙溶液中的离子浓度由大到小的顺序是c(NO3-)>c(NH4+)>c(H+)>c(OH-).X的含18个电子的气态氢化物丙可与空气构成一种环保型碱性燃料电池,电池工作时丙发生的电极反应方程式是N2H4-4e-+4OH-═N2+4H2O.(6)工业上用如图所示装置电 解Q元素的钠盐溶液丁,获得一种含Q元素的消毒剂.该反应的离子方程式是Cl-+H2O═ClO-+H2↑.