题目内容
 (1)盖斯定律认为:不管化学过程是一步完成或分数步完成,整个过程的总热效应相同. 试运用盖斯定律回答下列问题:
(1)盖斯定律认为:不管化学过程是一步完成或分数步完成,整个过程的总热效应相同. 试运用盖斯定律回答下列问题:已知:C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g);△H1=-Q1 kJ/mol,C2H5OH(g)=C2H5OH(l);
△H2=-Q2 kJ/mol,H2O(g)=H2O(l);△H3=-Q3 kJ/mol.若使23g液态无水酒精完全
燃烧,并恢复到室温,则整个过程中放出的热量为
(2)北京奥运会祥云火炬将中国传统文化、奥运精神以及 现代高科技融为一体.火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料.试回答下列问题:
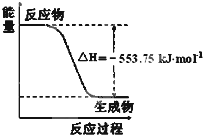
①如图是一定量丙烷完全燃烧生成CO2和1mol H2O(l)
过程中的能量变化图,请写出表示丙烷燃烧热的热化学方程式
考点:反应热和焓变,有关反应热的计算
专题:化学反应中的能量变化
分析:(1)依据热化学方程式,结合盖斯定律计算得到热化学方程式,即可解答;
(2)分析图象得到生成1mol水的焓变△H=-553.75KJ/mol;依据热化学方程式书写方法写出,注意物质聚集状态,对应量下的焓变.
(2)分析图象得到生成1mol水的焓变△H=-553.75KJ/mol;依据热化学方程式书写方法写出,注意物质聚集状态,对应量下的焓变.
解答:
解:(1)①C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g);△H1=-Q1 kJ/mol,
②C2H5OH(g)=C2H5OH(l);△H2=-Q2 kJ/mol,
③H2O(g)=H2O(l);△H3=-Q3 kJ/mol.
依据盖斯定律:①-②+3×③得到:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l);△H1=-(Q1-Q2+3Q3)kJ/mol,
若使23g液态无水酒精物质的量为0.5mol,完全燃烧,并恢复到室温,则整个过程中放出的热量为(0.5Q1-0.5Q2+1.5Q3 )KJ,△H=(-0.5Q1+0.5Q2-1.5Q3)KJ/mol
,故答案为:(0.5Q1-0.5Q2+1.5Q3);
(2)图象是一定量丙烷完全燃烧生成CO2和1mol H2O(l)过程中的能量变化图,反应放热△H=-553.75KJ/mol,则写出的热化学方程式为:
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l);△H1=-2215.0 kJ/mol,
故答案为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H1=-2215.0 kJ/mol.
②C2H5OH(g)=C2H5OH(l);△H2=-Q2 kJ/mol,
③H2O(g)=H2O(l);△H3=-Q3 kJ/mol.
依据盖斯定律:①-②+3×③得到:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l);△H1=-(Q1-Q2+3Q3)kJ/mol,
若使23g液态无水酒精物质的量为0.5mol,完全燃烧,并恢复到室温,则整个过程中放出的热量为(0.5Q1-0.5Q2+1.5Q3 )KJ,△H=(-0.5Q1+0.5Q2-1.5Q3)KJ/mol
,故答案为:(0.5Q1-0.5Q2+1.5Q3);
(2)图象是一定量丙烷完全燃烧生成CO2和1mol H2O(l)过程中的能量变化图,反应放热△H=-553.75KJ/mol,则写出的热化学方程式为:
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l);△H1=-2215.0 kJ/mol,
故答案为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H1=-2215.0 kJ/mol.
点评:本题考查了热化学方程式的书写、盖斯定律的运用,题目难度不大.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
有一空瓶的质量为W1g,该瓶充入空气后质量为W2g,相同条件下,充入某单质气体,其质量为W3g,则此单质气体的摩尔质量为( )
A、
| ||
B、
| ||
C、
| ||
D、
|


