题目内容
有一空瓶的质量为W1g,该瓶充入空气后质量为W2g,相同条件下,充入某单质气体,其质量为W3g,则此单质气体的摩尔质量为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
考点:摩尔质量
专题:计算题
分析:根据空气的质量计算空气的物质的量,相同条件下体积之比等于物质的量之比,所以单质气体的物质的量等于空气的物质的量,根据M=
计算该气体的摩尔质量.
| m |
| n |
解答:
解:有一空瓶的质量为W1 g,向该瓶充入空气后的质量为W2g,
则空气质量为(W2-W1)g,空气的物质的量为
=
mol,
相同条件下体积之比等于物质的量之比,所以该气体的物质的量为
mol,
相同条件下充入该气体,其质量为W3g,则该气体质量为(W3-W1)g.
所以该气体的摩尔质量为
=
g/mol.
故选:C.
则空气质量为(W2-W1)g,空气的物质的量为
| (W2-W1)g |
| 29g/mol |
| W2-W 1 |
| 29 |
相同条件下体积之比等于物质的量之比,所以该气体的物质的量为
| W2-W 1 |
| 29 |
相同条件下充入该气体,其质量为W3g,则该气体质量为(W3-W1)g.
所以该气体的摩尔质量为
| (W3-W1)g | ||
|
| 29(W 3-W 1) |
| W2-W 1 |
故选:C.
点评:本题考查阿伏伽德罗定律即推论、摩尔质量,难度不大,根据体积相同推断出物质的量相同是解题关键.

练习册系列答案
相关题目
下列各组物质不能使酸性高锰酸钾溶液退色的是( )
| A、二氧化硫 | B、乙炔 | C、苯 | D、乙烯 |
有一溶液可能含有SO42一、Br-、H2SO3、NH4+等微粒,对该溶液进行实验:不能确定在原溶液中一定存在的微粒是( )
①取少量溶液加热,放出的气体可以使品红溶液褪色;
②取原溶液加碱液使溶液呈碱性,加热,放出的气体能使湿润的红色石蕊试纸变蓝;
③取原溶液加氯水,溶液略显黄色,再加入BaCl2溶液,产生的白色沉淀不溶于稀硝酸.
①取少量溶液加热,放出的气体可以使品红溶液褪色;
②取原溶液加碱液使溶液呈碱性,加热,放出的气体能使湿润的红色石蕊试纸变蓝;
③取原溶液加氯水,溶液略显黄色,再加入BaCl2溶液,产生的白色沉淀不溶于稀硝酸.
| A、SO42- |
| B、Br- |
| C、H2SO3 |
| D、NH4+ |
用铝热法还原下列物质,制得金属各1摩尔,消耗铝最少的是( )
| A、MnO2 |
| B、FeO |
| C、Cr2O3 |
| D、V2O5 |
下列说法正确的是( )
| A、卤素单质都是有颜色的,而且颜色从F2→I2逐渐加深 |
| B、卤素原子半径逐渐增大是因为它们单质的熔、沸点逐渐升高 |
| C、卤化氢的稳定性和酸性都逐渐减弱 |
| D、卤素单质中从F2→I2前面的可以把后面的从它的卤化物溶液中置换出来 |
分别用0.20mol?L-1的AgNO3溶液10mL与相同体积的下列溶液恰好完全反应,则物质的量浓度最大的是( )
| A、KCl |
| B、MgCl2 |
| C、BaCl2 |
| D、AlCl3 |
下列电子式或结构式错误的是( )
A、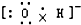 OH-的电子式 |
B、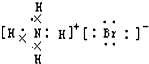 NH4Br的电子式 |
C、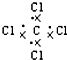 CCl4的电子式 |
| D、H2O的结构式H-O-H |
对滴有酚酞试液的下列溶液,操作后颜色变深的是( )
| A、AlCl3溶液加热 |
| B、Na2CO3溶液加热 |
| C、氨水中加入少量NH4Cl固体 |
| D、CH3COONa溶液中加入少量NaCl固体 |
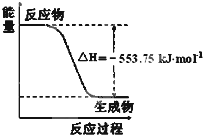 (1)盖斯定律认为:不管化学过程是一步完成或分数步完成,整个过程的总热效应相同. 试运用盖斯定律回答下列问题:
(1)盖斯定律认为:不管化学过程是一步完成或分数步完成,整个过程的总热效应相同. 试运用盖斯定律回答下列问题: