题目内容
6.现有下列10种物质:①H2O、②空气、③Mg、④CaO、⑤H2SO4、⑥Ca(OH)2、⑦CuSO4•5H2O、⑧碘酒、⑨C2H5OH、⑩NaHCO3.(将序号填在相应的空格内)其中,属于氧化物的是①④;属于酸的是⑤;属于碱的是⑥;属于盐的是⑦⑩.
分析 电离时生成的阳离子全部是H+的化合物属于酸;电离时生成的阴离子全部是OH-的化合物属于碱;有两种元素组成其中一种为氧的化合物为氧化物,
金属离子或铵根离子(NH4+)与酸根离子或非金属离子结合的化合物属于盐,酸、碱、盐、氧化物都是化合物,据此分析解答.
解答 解:①H2O含有两种元素一种为氧,属于氧化物;
②空气是混合物,不是化合物;
③Mg是单质,不是化合物;
④CaO含有Ca和O,两种元素,属于氧化物;
⑤H2SO4电离时生成的阳离子全部是H+的化合物属于酸;
⑥Ca(OH)2电离时生成的阴离子全部是OH-的化合物属于碱;
⑦CuSO4•5H2O金属离子与硫酸根离子组成的化合物属于盐;
⑧碘酒是混合物,不是化合物;
⑨C2H5OH为有机物,不属于酸、碱、盐、氧化物;
⑩NaHCO3是由钠离子与碳酸氢根离子构成的盐;
所以属于氧化物的是①④;属于酸的是⑤;属于碱的是⑥;属于盐的是⑦⑩;
故答案为:①④;⑤;⑥;⑦⑩.
点评 本题考查了物质的分类,明确酸、碱、盐、氧化物的概念是解题关键,题目难度不大.

练习册系列答案
相关题目
14.设阿伏加德罗常数为NA,则下列说法正确的是( )
| A. | 15g甲基(-CH3)所含有的电子数是9NA | |
| B. | 7.8g 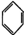 中含有的碳碳双键数为0.3NA 中含有的碳碳双键数为0.3NA | |
| C. | 1mol C2H5OH和1mol CH3CO18OH反应生成水的中子数为8NA | |
| D. | 标准状况下,11.2L己烷所含分子数为0.5NA |
1.某氧化物不溶于水,溶于熔化的NaOH中,生成易溶于水的化合物,向稀盐酸中滴加所生成化合物的水溶液,立即有白色沉淀产生,则原氧化物是( )
| A. | Al2O3 | B. | MgO | C. | SiO2 | D. | Fe2O3 |
11.下列表示物质结构的化学用语或模型正确的是( )
| A. | 硫酸的电离方程式:H2SO4=H2++SO42- | |
| B. | CO2的电子式: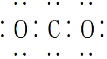 | |
| C. | Cl-离子的结构示意图: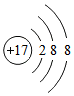 | |
| D. | 苯的结构简式:C6H6 |
18.下列关于芳香烃的叙述中不正确的是( )
| A. | 乙烷和甲苯中都含有甲基,甲苯可以被酸性KMnO4溶液氧化成苯甲酸,而乙烷不能被其氧化,说明苯环对侧链产生了影响 | |
| B. | 苯和浓硝酸、浓硫酸混合物在100~110℃才能生成二硝基苯,而甲苯在100℃时即可生成三硝基甲苯,说明甲基对苯环产生了影响 | |
| C. | 煤中含有苯和甲苯,可以用先干馏后分馏的方法把它们分离出来 | |
| D. | 除去苯中混入的少量甲苯可加入适量的酸性KMnO4溶液,充分反应后再加入足量的NaOH溶液,然后分液即可 |
15.下列说法正确的是( )
| A. | 化学反应的焓变与反应的途径有关 | |
| B. | 室温下,稀释0.1mol•L-1CH3COOH溶液,溶液的导电能力减弱 | |
| C. | 常温常压下,22.4L Cl2中含有的分子数为6.02×1023个 | |
| D. | 等质量的铜按a、b两种途径完全转化为Cu(NO3)2,途径a、b消耗的硝酸一样多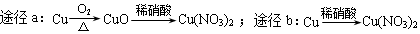 |
 aHCO3 +H2SO4 Na2CO3+HCl
aHCO3 +H2SO4 Na2CO3+HCl