题目内容
17.4.35g二氧化锰能与足量浓盐酸(密度为1.19g•cm-3、质量分数为36.5%)完全反应.求:(1)写出反应的化学方程式:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)浓盐酸中HCl的物质的量浓度:c(HCl)=11.9mol•L-1;
(3)被氧化的HCl的物质的量:n(HCl)=0.1mol;
(4)产生的氯气在标准状况下的体积:V(Cl2)=1.12L.
分析 发生MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,n(MnO2)=$\frac{4.35g}{87g/mol}$=0.05mol,结合反应可知,只有一半HCl作还原剂,结合c=$\frac{1000ρw}{M}$、V=nVm计算.
解答 解:(1)浓盐酸与二氧化锰反应生成氯气、氯化锰和水,反应为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)浓盐酸的密度为1.19g•cm-3、质量分数为36.5%,则浓度c=$\frac{1000×1.19×36.5%}{36.5}$=11.9mol•L-1,
故答案为:11.9mol•L-1;
(3)n(MnO2)=$\frac{4.35g}{87g/mol}$=0.05mol,则被氧化的HCl的物质的量为$\frac{0.05mol×(4-2)}{(1-0)}$=0.1mol,
故答案为:0.1mol;
(4)结合反应可知n(MnO2)=n(Cl2),产生的氯气在标准状况下的体积:V(Cl2)=0.05mol×22.4L/mol=1.12L,
故答案为:1.12L.
点评 本题考查氧化还原反应的计算,为高频考点,把握发生的反应、物质的量关系及电子守恒为解答的关键,侧重分析与计算能力的考查,注意盐酸的作用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.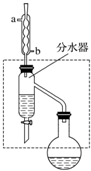 乙酸丁酯是重要的化工原料,具有水果香味.实验室制备乙酸丁酯的反应、装置示意图和有关信息如下:
乙酸丁酯是重要的化工原料,具有水果香味.实验室制备乙酸丁酯的反应、装置示意图和有关信息如下:
CH3COOH+CH3CH2CH2CH2OH$?_{浓H_{2}SO_{4}}^{△}$ CH3COOCH2CH2CH2CH3+H2O
(1)乙酸丁酯粗产品的制备
在干燥的50mL圆底烧瓶中,装入沸石,加入12.0mL正丁醇和16.0mL冰醋酸(过量),再加3~4滴浓硫酸.然后再安装分水器(作用:实验过程中不断分离除去反应生成的水)、冷凝管,然后小火加热.将烧瓶中反应后的混合物冷却与分水器的酯层合并.装置中冷水应从b(填“a”或“b”)口通入;通过分水器不断分离除去反应生成的水的目的是分离生成的水,使平衡正向移动,提高反应产率.
(2)乙酸丁酯的精制
将乙酸丁酯粗产品用如下的操作进行精制:①水洗、②蒸馏、③用无水MgSO4干燥、④用10%碳酸钠洗涤.
①正确的操作步骤是c(填标号).
A.①②③④B.③①④②C.④①③②D.③④①②
②在乙酸丁酯的精制中,用10%碳酸钠洗涤的主要目的是除去产品中含有的乙酸、硫酸等杂质.
③在洗涤、分液操作中,应充分振荡,然后静置,待分层后d(填标号).
a.直接将乙酸丁酯从分液漏斗的上口倒出
b.直接将乙酸丁酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸丁酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸丁酯从上口倒出
(3)计算产率
测量分水器内由乙酸与丁醇反应生成的水体积为1.8mL,假设在制取乙酸丁酯过程中反应物和生成物没有损失,且忽略副反应,乙酸丁酯的产率为77.1%.
 乙酸丁酯是重要的化工原料,具有水果香味.实验室制备乙酸丁酯的反应、装置示意图和有关信息如下:
乙酸丁酯是重要的化工原料,具有水果香味.实验室制备乙酸丁酯的反应、装置示意图和有关信息如下:CH3COOH+CH3CH2CH2CH2OH$?_{浓H_{2}SO_{4}}^{△}$ CH3COOCH2CH2CH2CH3+H2O
| 乙酸 | 正丁醇 | 乙酸丁酯 | |
| 熔点/℃ | 16.6 | -89.5 | -73.5 |
| 沸点/℃ | 117.9 | 117 | 126.0 |
| 密度/g•cm-3 | 1.1 | 0.80 | 0.88 |
在干燥的50mL圆底烧瓶中,装入沸石,加入12.0mL正丁醇和16.0mL冰醋酸(过量),再加3~4滴浓硫酸.然后再安装分水器(作用:实验过程中不断分离除去反应生成的水)、冷凝管,然后小火加热.将烧瓶中反应后的混合物冷却与分水器的酯层合并.装置中冷水应从b(填“a”或“b”)口通入;通过分水器不断分离除去反应生成的水的目的是分离生成的水,使平衡正向移动,提高反应产率.
(2)乙酸丁酯的精制
将乙酸丁酯粗产品用如下的操作进行精制:①水洗、②蒸馏、③用无水MgSO4干燥、④用10%碳酸钠洗涤.
①正确的操作步骤是c(填标号).
A.①②③④B.③①④②C.④①③②D.③④①②
②在乙酸丁酯的精制中,用10%碳酸钠洗涤的主要目的是除去产品中含有的乙酸、硫酸等杂质.
③在洗涤、分液操作中,应充分振荡,然后静置,待分层后d(填标号).
a.直接将乙酸丁酯从分液漏斗的上口倒出
b.直接将乙酸丁酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸丁酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸丁酯从上口倒出
(3)计算产率
测量分水器内由乙酸与丁醇反应生成的水体积为1.8mL,假设在制取乙酸丁酯过程中反应物和生成物没有损失,且忽略副反应,乙酸丁酯的产率为77.1%.
5.已知4NH3+5O2?4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,正确的关系是( )
| A. | 4 v(NH3)=5v(O2) | B. | 5v(O2)=6v(H2O) | C. | 4v(NH3)=6 v(H2O) | D. | 4v(O2)=5 v(NO) |
12.在CuO+H2 $\frac{\underline{\;高温\;}}{\;}$Cu+H2O反应中,下列说法正确的是( )
| A. | CuO是还原剂,被氧化 | |
| B. | H2是还原剂,被氧化 | |
| C. | H2O既不是氧化产物也不是还原产物 | |
| D. | Cu是还原产物,被还原 |
2.25℃时,水的电离达到平衡:H2O?H++OH-△H>0,下列叙述正确的是( )
| A. | 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 | |
| B. | 向水中加入氨水,平衡逆向移动,c(OH-)降低 | |
| C. | 向水中加入金属钠,平衡正向移动,c(H+)增大 | |
| D. | 将水加热,KW增大,pH不变 |
7.草木灰中含有可溶性钾盐(主要成分是K2SO4、K2CO3、KCl).某学生按下列操作提取草木灰中的钾盐:①取草木灰加水溶解;②过滤.取滤液;③蒸发滤液;④冷却结晶.
(1)在①、②、③、④的操作中需要用到玻璃棒是①②③(填序号).
(2)为检验草木灰中的离子,取少量晶体溶于水,并把溶液分成四份,完成以下实验报告(在横线上填写相关的内容):
(3)步骤ⅲ所得的结论,你认为是否正确?否(填是或否);为什么?加入氯化钡溶液,引入了Cl-.
(4)写出步骤ⅱ有关现象的离子方程式SO42-+Ba2+═BaSO4↓.
(1)在①、②、③、④的操作中需要用到玻璃棒是①②③(填序号).
(2)为检验草木灰中的离子,取少量晶体溶于水,并把溶液分成四份,完成以下实验报告(在横线上填写相关的内容):
| 实验步骤 | 实验现象 | 实验结论 |
ⅰ、取第一份溶液和适量稀盐酸加入下列装置的试管中,把澄清的石灰水加入烧杯中 | 气泡产生,澄清的石灰水变浑浊 | 证明含有碳酸根离子 |
| ⅱ、取第二份溶液,分别滴加稀盐酸和氯化钡 | 白色沉淀 | 证明含有硫酸根离子 |
| ⅲ、取第三份溶液加入过量BaCl2溶液,过滤,除去SO42-和CO32-,再滴加AgNO3溶液和稀硝酸 | 有白色沉淀生成 | 证明含有氯离子. |
| ⅳ、取第四份溶液进行焰色反应 | 透过蓝色钴玻璃火焰呈紫色 | 证明含有K+ |
(4)写出步骤ⅱ有关现象的离子方程式SO42-+Ba2+═BaSO4↓.