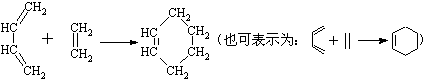
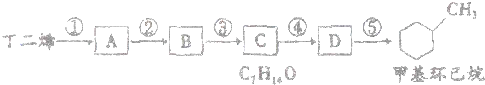
题目内容
将一定量有机物充分燃烧后的产物通入足量的石灰水中完全吸收,经过滤得到沉淀20g,滤液质量比原石灰水减少5.8g.该有机物不可能是( )
| A、C2H2 |
| B、HOCH2CH2OH |
| C、C2H6O |
| D、CH3OCH3 |
考点:有机物的推断
专题:烃及其衍生物的燃烧规律
分析:有机物燃烧完全燃烧生成CO2和H2O,通过足量的石灰水,发生反应:CO2+Ca(OH)2=CaCO3↓+H2O,得到沉淀20g为CaCO3质量,根据差量法计算生成碳酸钙的反应中导致溶液质量减少,再结合实际滤液质量减少计算燃烧生成水的质量,确定C、H原子数目之比,据此判断.
解答:
解:有机物燃烧产物有二氧化碳和水,将燃烧产物通过足量的石灰水,经过滤可得沉淀20g,应为CaCO3,
n(CO2)=n(CaCO3)=
=0.2mol,
CO2+Ca(OH)2=CaCO3↓+H2O 滤液减少的质量56
1mol 100g 56g
0.2mol 20g 11.2g
称量滤液时,其质量只比原石灰水减少5.8g,则生成水的质量应为11.2g-5.8g=5.4g,
则n(H)=2n(H2O)=
×2=0.6mol,
则有机物中N(C):N(H)=0.2mol:0.6mol=1:3,
选项中HOCH2CH2OH、C2H6O、CH3OCH3中C、H原子数目之比符合1:3,而C2H2不符合,
故选A.
n(CO2)=n(CaCO3)=
| 20g |
| 100g/mol |
CO2+Ca(OH)2=CaCO3↓+H2O 滤液减少的质量56
1mol 100g 56g
0.2mol 20g 11.2g
称量滤液时,其质量只比原石灰水减少5.8g,则生成水的质量应为11.2g-5.8g=5.4g,
则n(H)=2n(H2O)=
| 5.4g |
| 18g/mol |
则有机物中N(C):N(H)=0.2mol:0.6mol=1:3,
选项中HOCH2CH2OH、C2H6O、CH3OCH3中C、H原子数目之比符合1:3,而C2H2不符合,
故选A.
点评:本题考查有机物推断,难度中等,本题注意利用差量法计算水的质量为解答该题的关键,侧重考查学生的分析计算能力.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
下列溶液中的Cl-浓度与50mL 1mol?L-1 MgCl2溶液中的Cl-浓度相等的是( )
| A、150 mL 1 mol?L-1 NaCl溶液 |
| B、75 mL 2 mol?L-1 CaCl2溶液 |
| C、150 mL 2 mol?L-1 KCl溶液 |
| D、75 mL 1 mol?L-1 AlCl3溶液 |
生活中碰到的某些问题,常涉及到化学知识,下列说法不正确的是( )
| A、Mg(OH)2和Al(OH)3热分解生成的气态水可覆盖火焰、驱逐O2、稀释可燃气体,分解产物MgO和Al2O3能较快地与塑料燃烧过程中产生的酸性及腐蚀性气体反应,所以它们可以作为未来发展方向的无机阻燃剂 |
| B、近年来禽流感病毒H7N9时有病例报告,卫生部门强调要尽量避免接触活禽,个人也应加强消毒预防,其中消毒剂可以选用含氯消毒剂、酒精、双氧水等适宜的物质 |
| C、食品包装袋中常放入小袋的生石灰,目的是防止食品氧化变质 |
| D、碘的升华、溴水中萃取溴、石油的分馏均是物理变化 |
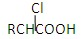
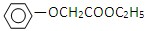 .
.
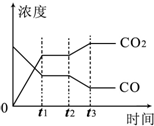 对于反应CO(g)+H2O(g)?H2(g)+CO2(g)
对于反应CO(g)+H2O(g)?H2(g)+CO2(g)