题目内容
16.X、Y、Z、R、W是原子序数依次增大的短周期主族元素,它们原子的最外层电子数之和为22.X与Z同主族,Y与W同主族,R最外层电子数是电子层数的2倍.下列叙述正确的是( )| A. | R与Z形成的是共价化合物 | |
| B. | 原子半径:W>R>Z | |
| C. | W的气态氢化物的热稳定性比Y的弱 | |
| D. | R的最高价氧化物的水化物酸性比W的强 |
分析 X、Y、Z、R、W是原子序数依次增大的短周期主族元素,R最外层电子数是电子层数的2倍,如果R有两个电子层则R是C元素、如果R有3个电子层则R是S元素,如果R是C元素,X和Z属于同一主族元素,则X只能是H元素,Z原子序数小于C,所以Z为Li元素,H和Li元素之间没有主族元素,所以R只能是S元素;
W原子序数大于R且为主族元素,所以W是Cl元素,Y和W同一主族且为短周期元素,所以Y是F元素;
这五种元素最外层电子数之和为22,S元素最外层有6个电子,则剩余四种元素最外层有16个电子,X与Z同主族,Y和W同一主族,X和Y最外层电子数是8,X最外层电子数是1,Z原子序数大于F元素,所以Z是Na元素,X为H或Li元素,结合原子结构以及周期率的递变规律解答该题.
解答 解:X、Y、Z、R、W是原子序数依次增大的短周期主族元素,R最外层电子数是电子层数的2倍,如果R有两个电子层则R是C元素、如果R有3个电子层则R是S元素,如果R是C元素,X和Z属于同一主族元素,则X只能是H元素,Z原子序数小于C,所以Z为Li元素,H和Li元素之间没有主族元素,所以R只能是S元素;
W原子序数大于R且为主族元素,所以W是Cl元素,Y和W同一主族且为短周期元素,所以Y是F元素;
这五种元素最外层电子数之和为22,S元素最外层有6个电子,则剩余四种元素最外层有16个电子,X与Z同主族,Y和W同一主族,X和Y最外层电子数是8,X最外层电子数是1,Z原子序数大于F元素,所以Z是Na元素,X为H或Li元素,
A.R是S元素,Z是Na元素,二者形成离子化合物,故A错误;
B.W是Cl元素,R是S元素,Z是Na元素,同周期元素从左到右原子半径逐渐减小,故B错误;
C.非金属性F>Cl,元素的非金属性越强,对应的氢化物越稳定,故C正确;
D.R是S元素,W是Cl元素,非金属性Cl>S,元素的非金属性越强,对应的最高价氧化物的水化物酸性越强,故D错误.
故选C.
点评 本题考查原子结构和元素性质,侧重考查分析、推断能力,正确判断R元素是解本题关键,易错选项是AB,注意X可能是H或Li元素,难度中等.

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案| A. | 灼烧的铁丝在氯气中燃烧,集气瓶内充满棕黄色烟雾 | |
| B. | 氢气在氯气中燃烧,集气瓶口有白雾 | |
| C. | 向盛水的烧杯中先加入过氧化钠,再滴加酚酞,最终溶液呈红色 | |
| D. | 将一块钠放在燃烧匙中加热,燃烧后得到白色固体 |
| A. | Ca2+ | B. | Ag+ | C. | H+ | D. | SO42- |
| A. | H2发生还原反应 | B. | H2是还原剂 | C. | Cl2被氧化 | D. | Cl2发生氧化反应 |
| A. | 高温有利于提高反应的转化率 | |
| B. | 高温可增大反应的限度 | |
| C. | 700K时反应催化剂活性最强,反应速率更快 | |
| D. | 高温才可以自发向右进行 |
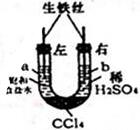 利用如图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间.下列说法不正确的是( )
利用如图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间.下列说法不正确的是( )| A. | a管发生吸氧腐蚀,b管发生析氢腐蚀 | |
| B. | 一段时间后,a管液面高于b管液面 | |
| C. | a处、b处溶液的pH都增大 | |
| D. | a、b两处具有相同的电极反应式:Fe-3e-═Fe3+ |
| A. | 在pH=1溶液中:NH4+、K+、ClO-、Cl- | |
| B. | 在含有大量CO32-溶液中:NH4+、Na+、Cl-、H+ | |
| C. | 有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br- | |
| D. | 在强碱溶液中:Na+、K+、CO32-、SiO32- |
| A. | 总反应可表示为2SO2+O2+2H2O$\stackrel{NO_{2}}{→}$2H2SO4 | |
| B. | 还可能发生的反应有4NO2+O2+2H2O→4HNO3 | |
| C. | NO2由反应N2+O2$\stackrel{放电}{→}$NO2生成 | |
| D. | 还可能发生的反应有4NO+3O2+2H2O→4HNO3 |