题目内容
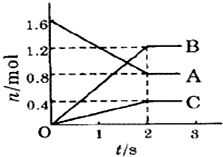 某温度下,在体积为5L的容器中,A、B、C三种物质物质的量随着时间变化的关系如图所示,则该反应的化学方程式为
某温度下,在体积为5L的容器中,A、B、C三种物质物质的量随着时间变化的关系如图所示,则该反应的化学方程式为考点:化学平衡建立的过程
专题:化学平衡专题
分析:根据在反应中减小的物质为反应物,增加的物质为生成物,各物质的物质的量的变化量之比等于反应中各物质的计量数之比,写出化学方程式;根据v=
计算反应速率;
| △c |
| t |
解答:
解:由图可知,在2min时,A的物质的量减小1.6mol-0.8mol=0.8mol,A为反应物,B的物质的量增加1.2mol,C的物质的量增加0.4mol,B、C为生成物,A、B、C的物质的量的变化量之比为0.8:1.2:0.4=2:3:1,
根据反应中的计量数之比等于变化的物质的物质的量之比,要写出反应方程式为:2A?3B+C,
2s内用A的浓度变化表示的平均反应速率为
mol/(L?s)=0.08mol/(L?s),
B的浓度变化表示的平均反应速率为
mol/(L?s)=0.12mol/(L?s),
故答案为:2A?3B+C;0.08mol/(L?s);0.12mol/(L?s).
根据反应中的计量数之比等于变化的物质的物质的量之比,要写出反应方程式为:2A?3B+C,
2s内用A的浓度变化表示的平均反应速率为
| ||
| 2 |
B的浓度变化表示的平均反应速率为
| ||
| 2 |
故答案为:2A?3B+C;0.08mol/(L?s);0.12mol/(L?s).
点评:本题主要考查了根据图象写化学方程式、计算反应速率,内容比较简单,注重对基础知识的考查.

练习册系列答案
相关题目
下列实验操作或装置(略去部分加持仪器)正确的是( )
A、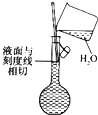 配制溶液 |
B、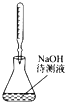 中和滴定 |
C、 制备乙酸乙酯 |
D、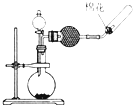 制备收集干燥的氨气 |
 ,单体为2-甲基-1,3-丁二烯(
,单体为2-甲基-1,3-丁二烯( ),该加聚反应的化学方程式为:
),该加聚反应的化学方程式为:
 为单体生产氯丁橡胶,试写出该反应的化学方程式:
为单体生产氯丁橡胶,试写出该反应的化学方程式: )按物质的量之比为1:1加聚,可生产丁苯橡胶,试写出丁苯橡胶的结构简式:
)按物质的量之比为1:1加聚,可生产丁苯橡胶,试写出丁苯橡胶的结构简式: ,形成该橡胶的单体为:
,形成该橡胶的单体为: