题目内容
一个重91.80g的洁净烧瓶中,加入两种饱和一元醛A和B的混合液4.68g,向混合液中加入足量的银氨溶液,并水浴加热,经充分反应后,过滤、仔细洗涤、干燥,称得瓶和固体质量共108.00g.已知B比A的相对分子质量大14.请计算:
(1)A和B各为什么醛
(2)B在混合物中的质量分数.
(1)A和B各为什么醛
(2)B在混合物中的质量分数.
考点:化学方程式的有关计算,有关混合物反应的计算
专题:计算题
分析:(1)假设A、B为甲醛以外的醛,令平均组成为CnH2nO,则有关系式:CnH2nO~2Ag,计算Ag的质量,再根据关系式计算n的值,又因B比A的相对分子质量大14,即A、B是相邻碳数的两醛,据此确定;
(2)利用平均C原子数目计算醛的物质的量之比,进而计算B的质量分数.
(2)利用平均C原子数目计算醛的物质的量之比,进而计算B的质量分数.
解答:
解:(1)因均为饱和一元醛,假设A、B为甲醛以外的醛,令平均组成为CnH2nO,则:
CnH2nO----2Ag
14n+16 2×108
4.68g 108.00g-91.80g=16.2g
(14n+2):216=4.68g:16.2g
解得n=3.3
又因B比A的相对分子质量大14,即A、B是相邻碳数的两醛,故A为丙醛,B为丁醛,
答:A为丙醛,B为丁醛.
(2)令丙醛、丁醛的物质的量分别为xmol、ymol,则:
=3.3,则x:y=7:3,
故丁醛的质量分数为
×100%=34.7%,
答:混合物中丁醛的质量分数为34.7%.
CnH2nO----2Ag
14n+16 2×108
4.68g 108.00g-91.80g=16.2g
(14n+2):216=4.68g:16.2g
解得n=3.3
又因B比A的相对分子质量大14,即A、B是相邻碳数的两醛,故A为丙醛,B为丁醛,
答:A为丙醛,B为丁醛.
(2)令丙醛、丁醛的物质的量分别为xmol、ymol,则:
| 3x+4y |
| x+y |
故丁醛的质量分数为
| 3mol×72g/mol |
| 3mol×72g/mol+7mol×58g/mol |
答:混合物中丁醛的质量分数为34.7%.
点评:本题考查混合物计算、有机物分子式确定等,难度中等,确定醛的组成是关键,题目数据计算比较麻烦,为易错点题目.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
张红同学出现了腹泻的症状,医生建议暂时不吃富含蛋白质和油脂的食物,张红同学应该选择的早餐( )
| A、油条和豆浆 |
| B、鸡蛋和牛奶 |
| C、馒头和稀饭 |
| D、肯德基和酸奶 |

 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产.生活中有着重要作用.请回答下列问题:
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产.生活中有着重要作用.请回答下列问题:
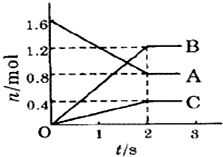 某温度下,在体积为5L的容器中,A、B、C三种物质物质的量随着时间变化的关系如图所示,则该反应的化学方程式为
某温度下,在体积为5L的容器中,A、B、C三种物质物质的量随着时间变化的关系如图所示,则该反应的化学方程式为