题目内容
7.NA表示阿伏加德罗常数,下列说法正确的是( )| A. | 2.24LCO或N2所含的电子数为1.4NA | |
| B. | 标准状况下,22.4升H2O中所含分子数小于NA | |
| C. | 常温常压下,33.6L氯气与56 g铁充分反应,转移的电子数为3NA | |
| D. | 常温常压下,1.8 g H2O含有的质子数为NA |
分析 A.气体的状况未知,不能计算其物质的量;B.标准状况下,水为液体;C.常温下,气体摩尔体积不是22.4L/mol;D.依据m=n×M计算水的物质的量即可.
解答 解:A.气体的状态不知道,无法计算其物质的量,故A错误;B.标准状况下,水是液体,不能利用气体摩尔体积计算其物质的量,故B错误;C.常温下,气体摩尔体积不是22.4L/mol,故氯气的物质的量不能计算,故C错误;D.1.8g水的物质的量为0.1mol,含有质子数是1mol,故D正确,故选D.
点评 本题考查了阿伏伽德罗常数的判断及计算,题目难度中等,掌握公式的使用和物质的结构、气体摩尔体积使用条件和对象是解题关键.

练习册系列答案
 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
17.一小块金属钠放入下列溶液中,既能产生气体又会生成白色沉淀的是( )
| A. | 稀硫酸 | B. | 氢氧化钾稀溶液 | C. | 硫酸铜溶液 | D. | 饱和石灰水溶液 |
2.对于铝热反应:Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,下列说法中正确的是( )
| A. | Fe元素的化合价升高 | |
| B. | 若27 g Al参加反应则有3 mol电子转移 | |
| C. | Fe2O3发生氧化反应 | |
| D. | Al被还原 |
12.以下关于甲烷分子说法中错误的是( )
| A. | 甲烷分子是由非极性键构成的分子 | |
| B. | 甲烷分子具有正四面体结构 | |
| C. | 甲烷分子中四个C-H键是完全相同的键 | |
| D. | 甲烷分子和CCl4分子具有相同的空间结构 |
19.某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合溶液(已知氯气和NaOH在一定温度下能发生反应:Cl2+2NaOH=NaCl+NaClO+H2O,3Cl2+6NaOH=5NaCl+NaClO3+3H2O),经测定ClO-与ClO3-的物质的量之比为1:2,则氯气与氢氧化钠反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为( )
| A. | 21:5 | B. | 11:3 | C. | 3:1 | D. | 4:1 |
16.下列物质能用来干燥CO2气体的是( )
| A. | 氢氧化钠 | B. | 碱石灰 | C. | 氧化钙 | D. | 浓H2SO4 |
17.下列有关化学用语或名称,表达错误的是( )
| A. | 丙烷分子的球棍模型图: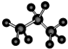 | B. | TNT的分子式:C7H5N3O6 | ||
| C. | 乙烯分子的比例模型: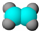 | D. | 苯乙醛的结构简式: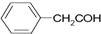 |