题目内容
19.某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合溶液(已知氯气和NaOH在一定温度下能发生反应:Cl2+2NaOH=NaCl+NaClO+H2O,3Cl2+6NaOH=5NaCl+NaClO3+3H2O),经测定ClO-与ClO3-的物质的量之比为1:2,则氯气与氢氧化钠反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为( )| A. | 21:5 | B. | 11:3 | C. | 3:1 | D. | 4:1 |
分析 Cl2生成ClO-与ClO3-是被氧化的过程,Cl2生成NaCl是被还原的过程,氧化还原反应中氧化剂和还原剂之间得失电子数目相等,根据ClO-与ClO3-的物质的量浓度之比可计算失去电子的总物质的量,进而可计算得到电子的总物质的量,可计算被还原的氯元素的物质的量,则可计算被还原的氯元素和被氧化的氯元素的物质的量之比.
解答 解:Cl2生成ClO-与ClO3-是被氧化的过程,化合价分别由0价升高为+1价和+5价,
ClO-与ClO3-的物质的量浓度之比为1:2,
则可设ClO-为1mol,ClO3-为2mol,被氧化的Cl共为3mol,
失去电子的总物质的量为1mol×(1-0)+2mol×(5-0)=11mol,
氧化还原反应中氧化剂和还原剂之间得失电子数目相等,
Cl2生成NaCl是被还原的过程,化合价由0价降低为-1价,
则得到电子的物质的量也应为11mol,
则被还原的Cl的物质的量为11mol,
所以被还原的氯元素和被氧化的氯元素的物质的量之比为11mol:3mol=11:3,
故选B.
点评 本题考查学生氧化还原反应的有关知识,注意电子守恒思想在解题中的运用,难度不大.

练习册系列答案
相关题目
9.下列有关烃的叙述正确的是( )
| A. | 分子通式为CnH2n+2的烃不一定是烷烃 | |
| B. | 烯烃在适宜的条件下只能发生加成反应,不能发生取代反应 | |
| C. | 在烷烃分子中,所有的化学键都是单键 | |
| D. | 分子式是C4H8的烃分子中一定含有碳碳双键 |
10.具有相同电子层数的三种元素X、Y、Z,已知它们最高价氧化物对应水化物的酸性强弱顺序是HXO4>H2YO4>H3ZO4.下列判断正确的是( )
| A. | 三种元素的原子半径:X>Y>Z | B. | 三种元素的单质的氧化性:X>Y>Z | ||
| C. | 阴离子的还原性:X->Y2->Z3- | D. | 气态氢化物的稳定性:X<Y<Z |
7.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 2.24LCO或N2所含的电子数为1.4NA | |
| B. | 标准状况下,22.4升H2O中所含分子数小于NA | |
| C. | 常温常压下,33.6L氯气与56 g铁充分反应,转移的电子数为3NA | |
| D. | 常温常压下,1.8 g H2O含有的质子数为NA |
11.工业制硫酸中,下列关于沸腾炉出来的气体主要成分描述中,最合理是( )
| A. | SO2、O2、N2 | B. | SO2、O2、N2、矿尘 | C. | SO2、SO3 | D. | Cl2、Ar、N2 |
8.下列反应中,不属于化合反应、分解反应、置换反应、复分解反应中的任一类型的是( )
| A. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | B. | C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2 | ||
| C. | Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O | D. | FeCl3+3NaOH═Fe(OH)3↓+3NaCl |
9.糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质.以下叙述正确的是( )
| A. | 植物油不能使溴的四氯化碳溶液褪色 | |
| B. | 蔗糖水解的最终产物是葡萄糖 | |
| C. | 葡萄糖能发生氧化反应和水解反应 | |
| D. | 蛋白质能发生水解最终生成氨基酸 |
 .
.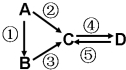 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系: