题目内容
阿伏加德罗常数约为6.02×1023mol-,下列说法正确的是( )
| A、0.05molC15H32分子中含有的共价键为2.3×6.02×1023 |
| B、常温下,42g 乙烯(CH2=CH2)和丁烯(CH2=CH-CH2-CH3)的混合气体中含有的碳原子数为2×6.02×1023 |
| C、0.3molNO2与足量水反应转移电子数为0.3×6.02×1023 |
| D、标准状况下,11.2L苯中所含原子总数为6×6.02×1023 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、C15H32为烷烃分子,结合烷烃结构简式共价键数;
B、乙烯(CH2=CH2)和丁烯(CH2=CH-CH2-CH3)的最简式相同为CH2,计算42gCH2中碳原子数;
C、依据反应3NO2+H2O=2HNO3+NO分析计算;
D、标准状况苯不是气体;
B、乙烯(CH2=CH2)和丁烯(CH2=CH-CH2-CH3)的最简式相同为CH2,计算42gCH2中碳原子数;
C、依据反应3NO2+H2O=2HNO3+NO分析计算;
D、标准状况苯不是气体;
解答:
解:A、C15H32为烷烃分子,结合烷烃结构简式共价键数=0.05mol×(15-1+32)×NA=2.3×6.02×1023,故A正确;
B、乙烯(CH2=CH2)和丁烯(CH2=CH-CH2-CH3)的最简式相同为CH2,计算42gCH2中碳原子数=
×1×NA=3×6.02×1023,故B错误;
C、依据反应3NO2+H2O=2HNO3+NO分析计算,3mol二氧化氮反应电子转移2mol,0.3molNO2与足量水反应转移电子数为0.2×6.02×1023,故C错误;
D、标准状况苯不是气体,11.2L苯物质的量不是0.5mol,故D错误;
故选A.
B、乙烯(CH2=CH2)和丁烯(CH2=CH-CH2-CH3)的最简式相同为CH2,计算42gCH2中碳原子数=
| 42g |
| 14g/mo |
C、依据反应3NO2+H2O=2HNO3+NO分析计算,3mol二氧化氮反应电子转移2mol,0.3molNO2与足量水反应转移电子数为0.2×6.02×1023,故C错误;
D、标准状况苯不是气体,11.2L苯物质的量不是0.5mol,故D错误;
故选A.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积条件应用,物质结构分析判断,氧化还原反应电子转移计算,掌握基础是关键,题目较较简单.

练习册系列答案
相关题目
某溶液中含有SO42-、CO32-、NH4+、M,且SO42-、CO32-、NH4+离子的物质的量之比为1:2:5,则离子M可能是( )
| A、H+ |
| B、K+ |
| C、C1- |
| D、Ba2+ |
下列反应常温时能自发进行,并既能用能量判据又能用熵判据解释的是( )
| A、HCl+NH3=NH4Cl |
| B、2Na+2H2O=2NaOH+H2↑ |
| C、2KClO3=2KCl+3O2↑ |
| D、Ba(OH)2?8H2O+2 NH4Cl=BaCl2+NH3↑+10H2O |
下列说法正确的是( )
| A、糖类都能发生水解反应 |
| B、通过地沟油(油脂)的碱性水解来制肥皂 |
| C、为减小溶液配制误差,容量瓶必须洗净并烘干后才能使用 |
| D、在鸡蛋白中滴入浓硫酸,会产生黄色物质,这就是蛋白质的颜色反应 |
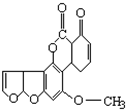 黄曲霉素的结构如下,1mol该化合物分别与H2、NaOH溶液反应最多消耗H2和NaOH的物质的量分别为( )
黄曲霉素的结构如下,1mol该化合物分别与H2、NaOH溶液反应最多消耗H2和NaOH的物质的量分别为( )| A、6mol,1mol |
| B、7mol,1mol |
| C、6mol,2mol |
| D、7mol,2mol |
下列有关实验操作或试剂贮存方法叙述正确的是( )
| A、配制FeCl3溶液时,将FeCl3溶解在较浓的盐酸中,再用水稀释到所需浓度 |
| B、实验室可将氯气溶于水配制成氯水长期保存,随时取用 |
| C、氢氟酸用玻璃瓶密封贮存 |
| D、NaOH溶液用磨口玻璃瓶加玻璃塞封存 |
在水溶液中能大量共存的一组是( )
| A、Fe2+ Al3+ ClO- Cl- |
| B、K+Fe3+OH- NO3- |
| C、NH4+ Na+ Br- SO42- |
| D、Na+ H+ SiO32- SO42- |
下列离子方程式书写正确的是( )
A、澄清石灰水与过量NaHCO3溶液混合:Ca2++OH-+HCO
| ||
B、向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O=HClO+HSO
| ||
| C、锌和稀硝酸的反应:Zn2++2H+=Zn2++H2 | ||
| D、CuSO4溶液吸收H2S气体:Cu2++H2S=CuS↓+2H+ |