题目内容
18.工业上用Na2SO3吸收尾气中的SO2使之转化为NaHSO3,再用SO2为原料设计的原电池电解(惰性电极)NaHSO3制取H2SO4,装置如图: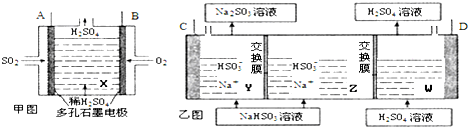
(1)甲图中B与乙图D极(填C或D)相连,进行电解时乙图Z中Na+向Y中移动(填Y或W);
(2)该电解池阴极的电极反应式2HSO3-+2e-═2SO32-+H2↑.
分析 (1)电解NaHSO3溶液制取H2SO4,阴极是水电离氢离子放电生成氢气,得到的氢氧根离子与亚硫酸氢根离子反应得到亚硫酸根,所以乙图C极为阴极,D为阳极,Na+向阴极区移动;
(2)乙图C极为阴极得电子发生还原反应.
解答 解:(1)电解NaHSO3溶液制取H2SO4,阴极是水电离氢离子放电生成氢气,得到的氢氧根离子与亚硫酸氢根离子反应得到亚硫酸根,所以乙图C极为阴极,D为阳极,则甲图中B为正极与乙图D相连,Na+向阴极Y区移动,故答案为:D;Y;
(2)乙图C极为阴极得电子发生还原反应,反应式为2HSO3-+2e-═2SO32-+H2↑,故答案为:2HSO3-+2e-═2SO32-+H2↑.
点评 本题涉及原电池、电解原理的考查,为高频考点,需要学生具备扎实的基础与分析解决问题的能力,注意把握二氧化硫的性质以及原电池、电解池的工作原理以及电极方程式的书写,难度较大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.镍是有机合成的重要催化剂,某化工厂有含镍催化剂废品(主要成分是镍、杂质是铁、铝单质及其化合物,还有少量难溶性杂质).某学习小组设计如下流程利用含镍催化剂废品制备硫酸镍晶体:

几种难溶碱开始沉淀和完全沉淀的pH:
回答下列问题:
(1)溶液①中含金属元素的离子是AlO2-.
(2)用离子方程式表示加入双氧水的目的2Fe2++H2O2+2H+=2Fe3++2H2O;双氧水可以用下列物质替代的是A.
A.氧气 B.漂白液 C.氯气 D.硝酸
(3)操作a和c需要共同的玻璃仪器是玻璃棒;操作C的名称是蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(4)如果加入双氧水量不足或“保温时间较短”,则所制备的产品可能含有的杂质为产品中混有绿矾;请选择合适的试剂,设计实验证明产品中是否含“杂质”取少量样品溶于蒸馏水,滴加酸性高锰酸钾溶液,若溶液紫色褪去,则产品中含有亚铁离子.
(5)含镍金属氢化物MH-Ni燃料电池是一种绝色环保电池,广泛应用于电动汽车.其中M代表储氢合金,MH代表金属氢化物,电解质溶液可以是KOH水溶液.它的充、放电反应为:xNi(OH)2+M $?_{放电}^{充电}$ MHx+xNiOOH;电池充电过程中阳极的电极反应式为Ni(OH)2+OH--e-=NiOOH+H2O,放电时负极的电极反应式为MHx+xOH--xe-=M++xH2O.

几种难溶碱开始沉淀和完全沉淀的pH:
| 沉淀物 | 开始沉淀 | 完全沉淀 |
| Al(OH)3 | 3.8 | 5.2 |
| Fe(OH)3 | 2.7 | 3.2 |
| Fe(OH)2 | 7.6 | 9.7 |
| Ni(OH)2 | 7.1 | 9.2 |
(1)溶液①中含金属元素的离子是AlO2-.
(2)用离子方程式表示加入双氧水的目的2Fe2++H2O2+2H+=2Fe3++2H2O;双氧水可以用下列物质替代的是A.
A.氧气 B.漂白液 C.氯气 D.硝酸
(3)操作a和c需要共同的玻璃仪器是玻璃棒;操作C的名称是蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(4)如果加入双氧水量不足或“保温时间较短”,则所制备的产品可能含有的杂质为产品中混有绿矾;请选择合适的试剂,设计实验证明产品中是否含“杂质”取少量样品溶于蒸馏水,滴加酸性高锰酸钾溶液,若溶液紫色褪去,则产品中含有亚铁离子.
(5)含镍金属氢化物MH-Ni燃料电池是一种绝色环保电池,广泛应用于电动汽车.其中M代表储氢合金,MH代表金属氢化物,电解质溶液可以是KOH水溶液.它的充、放电反应为:xNi(OH)2+M $?_{放电}^{充电}$ MHx+xNiOOH;电池充电过程中阳极的电极反应式为Ni(OH)2+OH--e-=NiOOH+H2O,放电时负极的电极反应式为MHx+xOH--xe-=M++xH2O.
9.下列仪器对应的名称正确的是 ( )
| A. |  三脚架 | B. |  酸式滴定管 酸式滴定管 | C. |  长颈漏斗 | D. |  蒸发皿 |
13.(Ⅰ)甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇. 某化学研究性学习小组模拟工业合成甲醇的反应(△H<0),在容积固定为2L的密闭容器内充入1molCO和 2molH2,加入合适催化剂(体积可以忽略不计)后在250°C开始反应,并用压力计监测容器内压强的变化如下:
(1)从反应开始到20min时,以CO表示的平均反应速率=0.0125mol/(L•min),
(2)该温度下平衡常数K=4(mol/L)-2,,若升高温度则K值减小(填“增大”、“减小”或“不变”);
(3)下列描述中能说明上述反应已达平衡的是BC;
A.2v (H2)正=v (CH3OH)逆
B.容器内气体的平均摩尔质量保持不变
C.容器中气体的压强保持不变
D.单位时间内生成 n molCO 的同时生成 2n molH2
(Ⅱ)在450℃并有催化剂存在下,于一容积恒定的密闭容器内进行下列反应:
2SO2(g)+O2(g)?2SO3(g)△H=-190kJ•mol-1
(1)该反应500℃时的平衡常数<450℃时的平衡常数(填“>”、“<”或“=”).
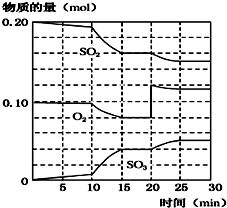
(2)450℃时,在一2L密闭容器中,将二氧化硫和氧化混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间是15~20 min和25~30 min.
(3)据图判断,反应进行至20min时,曲线发生变化的原因是增大O2浓度(通入O2);(用文字表达),10min到15min的曲线变化的原因可能是AB(填字母).
A.加了催化剂 B.缩小容器体积 C.降低温度 D.增加SO3物质的量
(4)欲提高SO2的转化率,下列措施可行的是b.(填字母)
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.升高温度.
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强/MPa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
(2)该温度下平衡常数K=4(mol/L)-2,,若升高温度则K值减小(填“增大”、“减小”或“不变”);
(3)下列描述中能说明上述反应已达平衡的是BC;
A.2v (H2)正=v (CH3OH)逆
B.容器内气体的平均摩尔质量保持不变
C.容器中气体的压强保持不变
D.单位时间内生成 n molCO 的同时生成 2n molH2
(Ⅱ)在450℃并有催化剂存在下,于一容积恒定的密闭容器内进行下列反应:

2SO2(g)+O2(g)?2SO3(g)△H=-190kJ•mol-1
(1)该反应500℃时的平衡常数<450℃时的平衡常数(填“>”、“<”或“=”).
(2)450℃时,在一2L密闭容器中,将二氧化硫和氧化混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间是15~20 min和25~30 min.
(3)据图判断,反应进行至20min时,曲线发生变化的原因是增大O2浓度(通入O2);(用文字表达),10min到15min的曲线变化的原因可能是AB(填字母).
A.加了催化剂 B.缩小容器体积 C.降低温度 D.增加SO3物质的量
(4)欲提高SO2的转化率,下列措施可行的是b.(填字母)
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.升高温度.
3.下列各组选项按照电解质-→非电解质-→单质-→混合物顺序排列的一项是( )
| A. | HCl-→SO3-→石墨-→液氧 | B. | NaCl-→乙醇-→铁-→空气 | ||
| C. | 蔗糖-→CuSO4-→氮气-→波尔多液 | D. | KCl-→NaNO3-→氯气-→石灰水 |
7.Cl2是纺织工业中常用的漂白剂.Na2S2O3可作漂白布匹后的“脱氯剂”,脱氯反应为S2O32-+Cl2++H20→SO42-+Cl-+H+ (未配平),下列对该反应的说法不正确的是( )
| A. | 反应每脱去1mol Cl2会生成1molSO42- | |
| B. | 脱氯反应后的溶液显酸性 | |
| C. | 根据该反应可判断还原性:S2O32->Cl- | |
| D. | 反应中硫元素发生了氧化反应 |
8.关于硅的下列叙述中,正确的是?( )
| A. | 晶体硅与金刚石分子都是正四面体结构 | |
| B. | 硅酸盐都不溶于水? | |
| C. | 硅与酸、碱都不能发生反应 | |
| D. | 原硅酸和硅酸对应的酸酐都是二氧化硅 |
