题目内容
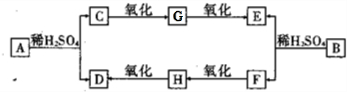
根据下图所示的关系填空,已知反应①③是工业生产中的重要反应,D、E常温下为气体,X常温下为无色液体,F是红棕色固体,又知C的焰色反应火焰呈黄色。
(1)物质X的化学式是________。
(2)化合物B中所包含的化学键有____________和___________。
(3)反应④的离子方程式为___________。反应②的化学方程式为____________,其中还原剂是________。
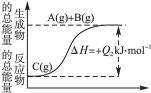
(4)已知每生成
(1)H2O (2)非极性键 离子键
(3)Fe2O3+6H+![]() 2Fe3++3H2O 2Na2O2+2H2O
2Fe3++3H2O 2Na2O2+2H2O![]() 4NaOH+O2↑ Na2O2
4NaOH+O2↑ Na2O2
(4) 4FeS2(s)+11O2(g)![]() 2Fe2O3(s)+8SO2(g);ΔH=-3 408 kJ·mol-1
2Fe2O3(s)+8SO2(g);ΔH=-3 408 kJ·mol-1
解析:本题是元素化合物的有关推断题,考查学生的知识综合能力。X常温下为无色液体,想到熟悉的物质H2O,红棕色固体为Fe2O3,焰色反应火焰呈黄色说明有Na元素。D、E常温下为气体,反应①③是工业生产中的重要反应,综合考虑说明A为FeS2,B为Na2O2,C是NaOH,D是O2,E是SO2,F是Fe2O3,G是SO3,M是H2SO4,I是Fe2(SO4)3溶液,C与I反应生成的是沉淀(J)和Na2SO4溶液,Fe(OH)3受热分解生成Fe2O3。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
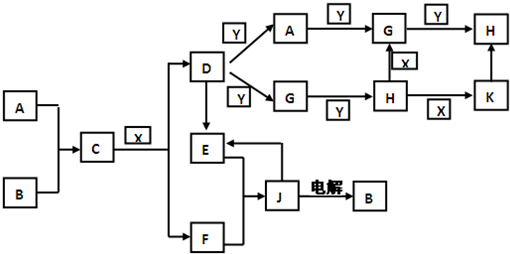
小学生10分钟应用题系列答案有①、②、③、④、⑤、⑥、⑦、⑧、⑨、⑩十种元素,原子序数依次增大,⑨、⑩处于第四周期,其余均为短周期元素。
(1)若②、⑦、⑧三种元素在周期表中相对位置如下
|
② |
|
|
|
|
|
|
⑦ |
⑧ |
②与⑧形成的液体化合物是常见的溶剂,则⑦元素在周期表中的位置是 ,②元素的氧化物的电子式是 ,②与⑧形成的化合物中存在的化学键是 ,则②、⑦、⑧三种元素最高价氧化物对应的水化物酸性由弱到强的顺序是 (用化学式表示)。⑦、⑧两种元素形成的阴离子半径大小顺序是 (用离子符号填)。
(2)若甲、己、丙、丁、戊均为上述短周期元素中组成的单质或化合物,且甲、乙、丙为无色气体,戊为红棕色气体。根据下图所示转化关系推测:

①写出反应a的化学方程式: 。
②写出戊与丁反应的化学方程式: 。
(3)若下图中A、B、C、D、E分别是上述10种元素组成的单质或化合物。
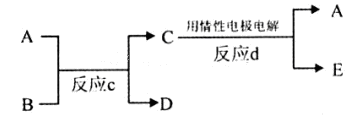
①若反应c是用A作电解池的阳极,电解B的水溶液,其中A是红色金属单质,E是具有黄绿色的气体。则反应d中阴极的电极反应式为: 。
②若反应c是在高温下进行的。其中B是暗红色固体,当物质C是一种两性化合物,则反应c的化学方程式为 。





 N2+3H2
N2+3H2 N2O4
N2O4