题目内容
20.某学生用优质大理石与稀盐酸反应制取CO2,实验结果如图所示,对于该图的叙述正确的是( )
| A. | 整个OC段反应过程中,反应速率逐渐增大 | |
| B. | BC段收集到的气体最多 | |
| C. | 因为OA段盐酸浓度最大,所以该段反应速率最快 | |
| D. | AB段反应快主要是因为反应放热导致的 |
分析 该题为化学反应速率图象题.解化学图象题,看图象:一看轴,看横坐标和纵坐标的意义.二看点,看图象上点的意义,看起点,转折点,终点.该题涉及影响化学反应速率的因素,解题时需考虑影响化学反应速率的两个因素:浓度,反应物浓度大,反应速率快;温度,温度高,反应速率快.从图象中曲线变化的关系知:曲线斜率表示反应速率.反应速率越大,反应速率越快;纵坐标越长,在该时间内收集到的气体越多.
解答 解:优质大理石与稀盐酸反应制取CO2原理为:CaCO3+2HCl═CaCl2+H2O+CO2↑该反应为放热反应.现象为:大理石逐渐溶解,有无色无味可使澄清石灰水变浑浊的气体产生.结合图象可知:
A.OC段表示随时间增加,从图象知,此时曲线斜率不是增大,故反应速率不是逐渐增大,故A错误;
B.从BC段纵坐标知:在该时间内收集到的气体不是最多,故B错误;
C.OA段因为盐酸浓度最大,但刚开始反应,放出的热量少,所以该段反应速率,虽浓度大反应快,但温度低,综合比较,不是最快,从图象知,此时曲线斜率不是最大,故反应速率不是最快.故C错误;
D.AB段,从图象知,此时曲线斜率最大,故反应速率最快,反应快是因为反应放热导致的,故D正确.
故选D.
点评 根据化学反应速率的定义,寻找化学图象中的曲线斜率与化学反应速率的关系,以及影响反应速率的因素,在图中怎样变化,是解题关键.

练习册系列答案
相关题目
11.化学与科学、技术、军事密切相关.下列说法正确的是( )
| A. | 光导纤维遇强碱会“断路” | |
| B. | 苹果放在空气中久置变黄和纸张久置变黄原理相似 | |
| C. | “辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料 | |
| D. | “歼-20”飞机上使用的碳纤维是一种新型的有机高分子材料 |
15.甲、乙两种非金属性质比较:①甲的单质熔、沸点比乙的低;②甲单质能氧化乙元素的阴离子;③最高价氧化物对应的水化物酸性比较,甲比乙的强;④与金属反应时甲原子得电子的数目比乙多;⑤甲单质比乙单质容易与氢气化合.其中能够说明甲比乙的非金属性强的是( )
| A. | ①②⑤ | B. | ③④⑤ | C. | ②③⑤ | D. | ②③④⑤ |
5.S-诱抗素可保证盆栽鲜花盛开,其分子结构如图,下列说法正确的是( )
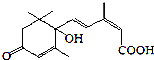

| A. | 该物质的分子式为C15H22O4 | |
| B. | 该物质环上的二氯代物共有3种 | |
| C. | 1mol该物质最多能与2 mol NaOH完全反应 | |
| D. | 该物质能发生取代、加成、氧化等反应 |
12.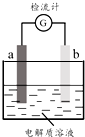 30℃时,利用图装置进行实验,结果记录如下表所示:
30℃时,利用图装置进行实验,结果记录如下表所示:
下列说法不正确的是( )
 30℃时,利用图装置进行实验,结果记录如下表所示:
30℃时,利用图装置进行实验,结果记录如下表所示:| 实验 | a电极 | b电极 | 电解质溶液 | 现象 |
| I | Cu | Zn | 稀H2SO4 | 检流计指针向左偏转 |
| Ⅱ | Fe | Al | 稀H2SO4 | 检流计指针向左偏转 |
| Ⅲ | Fe | Al | 浓H2SO4 | 检流计指针先向左偏转,后逐渐归零,a电极表面逐渐变黑,b电极表面逐渐变白 |
| Ⅳ | Fe | Al | 浓HNO3 | 检流计指针迅速向右偏转,a电极逐渐溶解,b电极表面逐渐变白 |
| A. | Ⅱ中Al为负极,其电极反应是:Al-3e-═Al3+ | |
| B. | Ⅱ中的现象说明Fe和Al表面形成致密的氧化膜,阻止了电极反应的进行 | |
| C. | Ⅳ中Fe为负极,发生了氧化反应 | |
| D. | 上述实验表明:相同条件下,Fe在浓HNO3中更稳定,Al在浓H2SO4中更稳定 |
9. 如图所示的微生物燃料电池在净化废水的同时能回收能源或得到有价值的化学产品.下列有关说法不正确的是( )
如图所示的微生物燃料电池在净化废水的同时能回收能源或得到有价值的化学产品.下列有关说法不正确的是( )
 如图所示的微生物燃料电池在净化废水的同时能回收能源或得到有价值的化学产品.下列有关说法不正确的是( )
如图所示的微生物燃料电池在净化废水的同时能回收能源或得到有价值的化学产品.下列有关说法不正确的是( )| A. | b极为正极,发生还原反应 | |
| B. | 负极的电极反应式为CH3CHO-10e-+3H2O═2CO2↑+10H+ | |
| C. | 理论上处理l mol Cr2O72-时有l4mool H+从交换膜左侧向右侧迁移 | |
| D. | 放电时,交换膜右侧生物菌周围溶液的pH增大 |
10.在体积为V L的恒容密闭容器中加入6mol CO和H2的混合气体,在不同条件下发生反应:CO(g)+2H2(g)?CH3OH(g).图1表示有、无催化剂时反应的能量变化,图2表示平衡时CH3OH的体积分数随起始n(CO):n(H2)的变化关系.下列叙述正确的是( )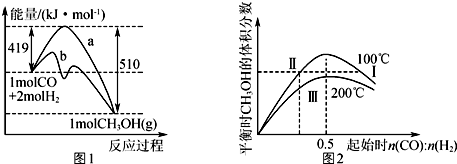

| A. | 正反应的△H=91 kJ•mol-1,曲线b表示使用了催化剂 | |
| B. | 正反应速率v正:v正(状态Ⅱ)<v正(状态Ⅲ) | |
| C. | 平衡时CO的转化率:α(CO,状态Ⅰ)<α(CO,状态Ⅱ) | |
| D. | n(CO):n(H2)=0.5时,平衡时CH3OH的物质的量浓度:c(CH3OH,1 00℃)<c(CH3OH,200℃) |
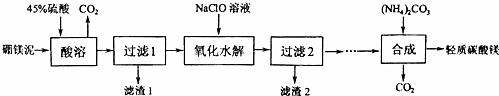
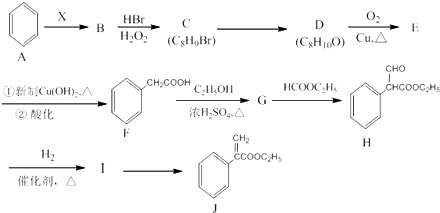
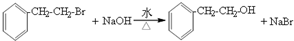 .
.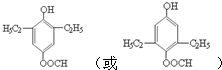 (任写一种即可).
(任写一种即可).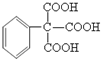 的合成路线流程图(无机试剂任选).
的合成路线流程图(无机试剂任选).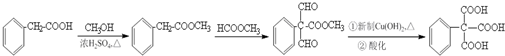 .
.