题目内容
12.反应C(s)+H2O?CO(g)+H2(g)△H>0,达到平衡时,下列说法正确的是( )| A. | 加入催化剂,平衡常数不变 | |
| B. | 减小容器体积,正、逆反应速率均减小 | |
| C. | 增大C的量,H2O的转化率增大 | |
| D. | 升高温度,平衡向逆反应方向移动 |
分析 A.平衡常数只与温度有关;
B.减小容器体积,压强增大;
C.C为纯固体;
D.该反应为吸热反应.
解答 解:A.平衡常数只与温度有关,则加入催化剂,平衡常数不变,故A正确;
B.减小容器体积,压强增大,则正逆反应速率均增大,故B错误;
C.C为纯固体,增大C的量,平衡不移动,故C错误;
D.该反应为吸热反应,则升高温度,平衡向正反应方向移动,故D错误;
故选A.
点评 本题考查化学平衡的影响因素,为高频考点,把握温度、压强对平衡的影响为解答的关键,侧重分析与应用能力的考查,注意平衡移动原理的应用,题目难度不大.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
3.下表中,对陈述I、II的正确性及两者间是否具有因果关系的判断都正确的是( )
| 选项 | 陈述I | 陈述II | 判断 |
| A | 氢氧化铝可用于治疗胃酸过多 | Al(OH)3可与盐酸反应 | I对,II对,有 |
| B | SiO2可用作光导纤维 | SO2是良好的半导体 | I对,II对,有 |
| C | Al2O3作耐火材料 | Al2O3具有高熔点 | I对,II错,无 |
| D | HF可用来蚀刻玻璃 | HF是强酸 | I对,II对,无 |
| A. | A | B. | B | C. | C | D. | D |
3.一些常见有机物的转化如图下列说法正确的是( )


| A. | 上述有机物中只有C6H12O6属于糖类物质 | |
| B. | 转化1可在人体内完成,该催化剂属于蛋白质 | |
| C. | 物质C和油脂类物质互为同系物 | |
| D. | 物质A和B都属于电解质 |
20.下列溶液中,与100ml 0.5mol/L NaCl溶液所含的Cl-的物质的量浓度相同的是( )
| A. | 100 ml 0.5 mol/L MgCl2 溶液 | B. | 200 ml 0.25 mol/L HCl溶液 | ||
| C. | 50 ml 1 mol/L NaCl溶液 | D. | 200 ml 0.25 mol/L CaCl2溶液 |
7.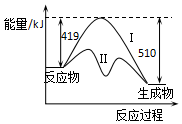 已知:CO(g)+2H2(g)?CH3OH(g)△H,反应过程中生成1mol CH3OH(g)的能量变化如图所示.曲线Ⅰ、Ⅱ分别表示无或有催化剂两种情况.下列判断正确的是( )
已知:CO(g)+2H2(g)?CH3OH(g)△H,反应过程中生成1mol CH3OH(g)的能量变化如图所示.曲线Ⅰ、Ⅱ分别表示无或有催化剂两种情况.下列判断正确的是( )
 已知:CO(g)+2H2(g)?CH3OH(g)△H,反应过程中生成1mol CH3OH(g)的能量变化如图所示.曲线Ⅰ、Ⅱ分别表示无或有催化剂两种情况.下列判断正确的是( )
已知:CO(g)+2H2(g)?CH3OH(g)△H,反应过程中生成1mol CH3OH(g)的能量变化如图所示.曲线Ⅰ、Ⅱ分别表示无或有催化剂两种情况.下列判断正确的是( )| A. | 加入催化剂,△H变小 | |
| B. | △H=+91 kJ/mol | |
| C. | 生成1molCH3OH(l)时,△H值增大 | |
| D. | 反应物的总能量大于生成物的总能量 |
17.下列反应中,△S<0的是( )
| A. | H2(g)+Br2(g)?2HBr(g) | B. | 2N2O5(g)=4NO2(g)+O2(g) | ||
| C. | 2SO2(g)+O2?2SO3(g) | D. | CaCO3(s)=CaO(s)+CO2(g) |
4.铝分别与足量的稀盐酸和氢氧化钠溶液反应,当两个反应放出的气体在相同状况下体积相等时,反应中消耗的HCl和NaOH的物质的量之比是( )
| A. | 1:1 | B. | 2:1 | C. | 1:3 | D. | 3:1 |
1.下列各物质中,所含分子数相同的是( )
| A. | 10gCH4和 10gO2 | B. | 11.2LN2(标准状况)和 11g CO2 | ||
| C. | 9 g H2O 和 0.5mol Cl2 | D. | 224mL H2(标准状况)和 0.1mol N2 |
2.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | pH=12的溶液中:Al3+、Na+、CH3COO-、SO32- | |
| B. | 无色溶液中:Cu2+、Ca2+、HSO3-、NO3- | |
| C. | 新制氯水中:NH4+、Fe3+、SO42-、Cl- | |
| D. | 磷酸溶液中:Ba2+、Mg2+、CO32-、Br- |