题目内容
4.铝分别与足量的稀盐酸和氢氧化钠溶液反应,当两个反应放出的气体在相同状况下体积相等时,反应中消耗的HCl和NaOH的物质的量之比是( )| A. | 1:1 | B. | 2:1 | C. | 1:3 | D. | 3:1 |
分析 足量的稀盐酸和氢氧化钠溶液反应,则Al完全反应,两个反应放出的气体在相同状况下体积相等时,结合反应分析.
解答 解:足量的稀盐酸和氢氧化钠溶液反应,则Al完全反应,两个反应放出的气体在相同状况下体积相等时,
由2Al~2NaOH~6HCl~3H2可知,
反应中消耗的HCl和NaOH的物质的量之比为6mol:2mol=3:1,
故选D.
点评 本题考查Al的化学性质,把握铝与酸、碱的反应为解答的关键,注意酸碱足量,金属完全反应,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
15.最新“人工固氮”的研究报道:常温常压、光照条件下,N2在催化剂表面与水发生反应:2N2(g)+6H2O(l)?4NH3 (g)+3O2(g)-Q(Q>0),如果反应的平衡常数K值变大,该反应( )
| A. | 一定向正反应方向移动 | |
| B. | 一定向逆反应方向移动 | |
| C. | 在平衡移动时正反应速率先减小后增大 | |
| D. | 在平衡移动时逆反应速率先增大后减小 |
15.下列说法不正确的是( )
| A. | 钠、铁和铜一样都能在氯气中燃烧生成金属氯化物 | |
| B. | 硫酸铜溶液中加入足量铝粉,充分振荡溶液颜色将由蓝色变成无色,同时有红色物质析出 | |
| C. | 实现SO2→S的变化需要氧化剂才能实现 | |
| D. | 氯水具有杀菌、漂白作用是因氯水中含有强氧化性的次氯酸 |
12.反应C(s)+H2O?CO(g)+H2(g)△H>0,达到平衡时,下列说法正确的是( )
| A. | 加入催化剂,平衡常数不变 | |
| B. | 减小容器体积,正、逆反应速率均减小 | |
| C. | 增大C的量,H2O的转化率增大 | |
| D. | 升高温度,平衡向逆反应方向移动 |
19.pH=4的盐酸和氯化铵溶液中,水的电离程度前者与后者比较( )
| A. | 大于 | B. | 等于 | C. | 小于 | D. | 无法确定 |
9.已知单质碘受热易升华.从海带中提取碘的实验过程中涉及下列操作正确的是( )
| A. | 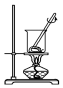 灼烧海带 | B. | 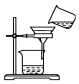 过滤得含I-的溶液 | ||
| C. | 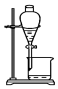 放出碘的苯溶液 | D. | 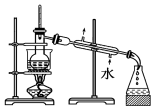 分离碘并回收苯 |
16.下列各组中的反应,属于同一反应类型的是( )
| A. | 乙烷与氯气在光照下反应生成氯乙烷;乙烯与氯化氢反应生成氯乙烷 | |
| B. | 甲苯硝化生成对硝基甲苯;乙醇催化氧化生成乙醛 | |
| C. | 苯使溴水褪色;丙烯使溴水褪色 | |
| D. | 乙酸和乙醇生成乙酸乙酯;苯与液溴反应生成溴苯 |
13.在A(g)+B(g)=C(g)+2D(g)反应中,下列表示的反应速率最快的是( )
| A. | v(A)═0.1mol•L-1•min | B. | v(B)═0.2 mol•L-1•min | ||
| C. | v(C)═0.3 mol•L-1•min | D. | v(D)═0.4mol•L-1•min |
14.化学与社会、生产、生活密切相关.下列说法中不正确的是( )
| A. | 煤炭经气化、液化和干馏等过程,可以转化为淸洁能源 | |
| B. | 利用二氧化碳来制造全降解塑料,可以缓解温室效应 | |
| C. | 高纯硅可用于制造太阳能电池、计算机芯片和光异纤维 | |
| D. | 在医疗上.可用碳酸氢钠治疗胃酸过多症 |