题目内容
8.下列有关物质的表达式正确的是( )| A. | 乙炔分子的比例模型  | B. | 溴乙烷的电子式: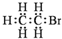 | ||
| C. | 2-氯丙烷的结构简式:CH3CHClCH3 | D. | 丙烯的键线式: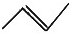 |
分析 A.乙炔是直线型分子;
B.溴乙烷中漏写溴原子上孤电子对;
C.2-氯丙烷,在2号碳上含有1个氯原子,根据烷烃命名书写;
D.键线式是以短线代替碳碳共价键,分子中的碳氢键、碳原子及与碳原子相连的氢原子均省略,其它杂原子及与杂原子相连的氢原子须保留,交点和端点表示碳原子,由H原子来饱和使碳达到4价结构.
解答 解:A.乙炔是直线型分子,四个原子处于同一直线上,故A错误;
B.溴乙烷的电子式为: ,故B错误;
,故B错误;
C. 2-氯丙烷,在2号碳上含有1个氯原子,结构简式为:CH3CHClCH3,故C正确;
D.丙烯的结构式为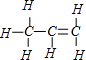 ,故其键线式为
,故其键线式为 ,故D错误.
,故D错误.
故选C.
点评 本题考查化学用语,难度不大,易错选项是B,书写电子式时易漏掉孤电子对,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.设NA表示阿伏加德罗常数的值,下列叙述中不正确的是( )
| A. | 1 mol Cl2与足量Ca(OH)2溶液反应,转移的电子数为NA | |
| B. | 1 mol碳烯(:CH2)所含的电子数目为6 NA | |
| C. | 常温常压下,11.2 L甲烷中含有的氢原子数小于2 NA | |
| D. | 某温度时,1 L pH=6的纯水中含OH-数为10-6NA |
19.下列说法正确的是( )
| A. | 已知C-C键可以绕键轴自由旋转,结构简式为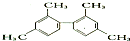 的分子中至少有11个碳原子处于同一平面上 的分子中至少有11个碳原子处于同一平面上 | |
| B. | 苯中含有杂质苯酚,可用浓溴水来除杂 | |
| C. | 1mo1 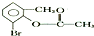 在一定条件下与足量NaOH溶液反应,最多消耗3 mol NaOH 在一定条件下与足量NaOH溶液反应,最多消耗3 mol NaOH | |
| D. | 按系统命名法,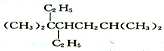 的名称为3,3,6一三甲基-4-乙基庚烷 的名称为3,3,6一三甲基-4-乙基庚烷 |
16. 某酯是一种食用香料,其结构简式如图所示,有关该酯叙述正确的是( )
某酯是一种食用香料,其结构简式如图所示,有关该酯叙述正确的是( )
 某酯是一种食用香料,其结构简式如图所示,有关该酯叙述正确的是( )
某酯是一种食用香料,其结构简式如图所示,有关该酯叙述正确的是( )| A. | 分子式为C12H18O2 | |
| B. | 能发生加成反应、取代反应和消去反应 | |
| C. | 能使酸性KMn04溶液和溴水褪色,且褪色原理相同 | |
| D. | 1mol该有机物在一定条件下和H2反应,共消耗H2为2mol |
3. 我国“蛟龙”号载入潜水器进行第五次下潜试验,最大深度达到7062米,并完全返回.其动力电源是Al-AgO电池,原理如图所示.下列说法中正确的是( )
我国“蛟龙”号载入潜水器进行第五次下潜试验,最大深度达到7062米,并完全返回.其动力电源是Al-AgO电池,原理如图所示.下列说法中正确的是( )
 我国“蛟龙”号载入潜水器进行第五次下潜试验,最大深度达到7062米,并完全返回.其动力电源是Al-AgO电池,原理如图所示.下列说法中正确的是( )
我国“蛟龙”号载入潜水器进行第五次下潜试验,最大深度达到7062米,并完全返回.其动力电源是Al-AgO电池,原理如图所示.下列说法中正确的是( )| A. | Al电极是该电池的正极 | |
| B. | Ag在AgO/Ag电极上发生氧化反应 | |
| C. | 该电池负极反应是2Al-6e-+8OH-═2AlO2-+4H2O | |
| D. | AgO/Ag电极溶液中的pH减小 |
13.有机物 又名萘,则萘的化学式为( )
又名萘,则萘的化学式为( )
 又名萘,则萘的化学式为( )
又名萘,则萘的化学式为( )| A. | C10H10 | B. | C10H8 | C. | C12H10 | D. | C10H12 |
4.下列微粒的电子式或化合物的形成过程不正确的是( )
| A. | 氯原子: | B. | OH-离子: | ||
| C. | NH3 | D. | HCl的形成过程: |
5.不同的金属在冶炼方法上也有所不同,下列说法正确的是( )
| A. | 钒、铬、锰、铁等难熔金属通常采用铝热法炼制 | |
| B. | 炼钢和炼铁都是采用还原剂将铁从其化合物中还原出来,区别在于炼钢时选用的还原剂的还原性更强 | |
| C. | 由于钠、镁、铝等金属化学性质太活泼,人们通常采用电解熔融状态下的氯化物的方式来获取它们的单质 | |
| D. | 炼铁时加入的焦炭除了提供热量外,还用来制造还原剂一氧化碳 |
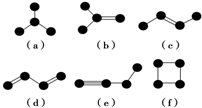 如图是由4个碳原子结合成的6种有机物(氢原子没有画出).
如图是由4个碳原子结合成的6种有机物(氢原子没有画出).