题目内容
18.设NA表示阿伏加德罗常数的值,下列叙述中不正确的是( )| A. | 1 mol Cl2与足量Ca(OH)2溶液反应,转移的电子数为NA | |
| B. | 1 mol碳烯(:CH2)所含的电子数目为6 NA | |
| C. | 常温常压下,11.2 L甲烷中含有的氢原子数小于2 NA | |
| D. | 某温度时,1 L pH=6的纯水中含OH-数为10-6NA |
分析 A、氯气和碱的反应为歧化反应;
B、碳烯(:CH2)中含8个电子;
C、常温常压下,气体摩尔体积大于22.4L/mol;
D、纯水显中性.
解答 解:A、氯气和碱的反应为歧化反应,故1mol氯气转移1mol电子即NA个,故A正确;
B、碳烯(:CH2)中含8个电子,故1mol碳烯中含8NA个电子,故B错误;
C、常温常压下,气体摩尔体积大于22.4L/mol,故11.2L甲烷的物质的量小于0.5mol,则含有的氢原子数小于2NA个,故C正确;
D、纯水显中性,故水中的氢氧根的个数等于氢离子的个数,即为10-6NA,故D正确.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
相关题目
8.最近,国际机构正在给第113号元素进行命名,该元素的某种原子有一个“巨大”的原子核,包含113个质子和173个中子.关于该原子的说法错误的是( )
| A. | 核电荷数为113 | B. | 质量数为286 | C. | 核外电子数为173 | D. | 化学性质不稳定 |
9.下列化学用语正确的是( )
| A. | CH3OOCCH3名称为甲酸乙酯 | |
| B. | 次氯酸的电子式  | |
| C. | 17Cl原子3p亚层有一个未成对电子 | |
| D. | 碳原子最外层电子云有两种不同的伸展方向 |
6.不能用于比较Na与Al金属性相对强弱的事实是( )
| A. | 最高价氧化物对应水化物的碱性强弱 | |
| B. | Na和AlCl3溶液反应 | |
| C. | 单质与H2O反应的难易程度 | |
| D. | 比较同浓度NaCl和AlCl3的pH大小 |
3.下列实验现象与实验解释正确的是( )
| 编号 | 实验操作 | 实验解释 |
| A | 用蒸馏法分离碘CCl4溶液 | 利用碘易升华原理 |
| B | 用KMnO4除去葡萄糖溶液中的乙醇 | KMnO4可以氧化乙醇 |
| C | 蔗糖中加入浓硫酸会变黑、放热、膨胀,放出刺激性气体 | 浓硫酸具有脱水性、吸水性和强氧化性 |
| D | 向某溶液中加入用盐酸酸化的Ba(NO3)2产生白色沉淀 | 说明此溶液中含有SO42- |
| A. | A | B. | B | C. | C | D. | D |
10.设NA为阿伏加德罗常数的值.下列叙述正确的是(C-12 N-14 O-16)( )
| A. | 标准状况下,11.2 L甲烷中含有的碳氢键数目为2NA | |
| B. | 常温下,1L 0.1mol/L的Na2CO3溶液中含有OH-离子数为0.1NA | |
| C. | 常温常压下,28 g N2、CO的混合气体中含有N2分子数为0.5NA | |
| D. | 标准状况下,22.4 L Cl2与足量NaOH溶液反应,转移的电子数为2NA |
7.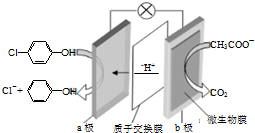 现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(
现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚( 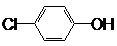 ),其原理如图所示,下列说法正确的是( )
),其原理如图所示,下列说法正确的是( )
 现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(
现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(  ),其原理如图所示,下列说法正确的是( )
),其原理如图所示,下列说法正确的是( )| A. | b为电池的正极,发生还原反应 | |
| B. | 电流从b极经导线、小灯泡流向a极+2e-+H+=Cl-+ | |
| C. | a极的电极反应式为: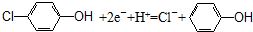 | |
| D. | 当外电路中有0.2mole-转移时,a极区增加的H+的个数为0.2NA |
8.下列有关物质的表达式正确的是( )
| A. | 乙炔分子的比例模型  | B. | 溴乙烷的电子式: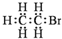 | ||
| C. | 2-氯丙烷的结构简式:CH3CHClCH3 | D. | 丙烯的键线式: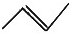 |
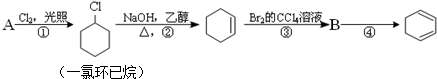
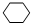 ,①的反应类型是取代反应,③的反应类型是加成反应.反应④的化学方程式是
,①的反应类型是取代反应,③的反应类型是加成反应.反应④的化学方程式是