题目内容
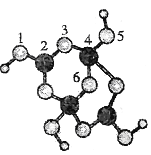
【题目】硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如下图所示:下列叙述正确的是
A.Xm-的化学式为B4O8H42-
B.硼原子轨道的杂化类型有sp2、 sp3
C.配位键存在于4、6原子之间
D.硼砂晶体中有离子键、配位键两种化学键
【答案】B
【解析】
A.观察模型,1,3,5,6代表氧原子,2,4代表B原子,可知Xm-是(H4B4O9)m-,依据化合价H为+1,B为+3,O为-2,可得m=2,则Xm-的化学式为:(H4B4O9)2-,故A错误;
B.根据图知,B原子价层电子对个数是3的采用sp2杂化、是4的采用sp3杂化,故B正确;
C.含有空轨道的原子和含有孤电子对的原子之间易形成配位键,B原子含有空轨道、O原子含有孤电子对,4,5(或5,4)原子之间存在配位键,故C错误;
D.硼砂晶体中有离子键、配位键和共价键三种化学键,故D错误;
故选B。
【点晴】
本题考物质结构和性质,涉及配合物成键情况、原子杂化、等知识点,为高频考点,知道配位键的构成条件,会判断原子杂化方式是解答关键。根据价层电子对互斥理论确定分子空间构型及中心原子杂化方式,价层电子对个数=σ键个数+孤电子对个数,σ键个数=配原子个数,孤电子对个数=![]() (a-xb),a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数,1,3,5,6代表氧原子,2,4代表B原子,2号B形成3个键,则B原子为sp2杂化,4号B形成4个键,则B原子为sp3杂化;3号氧原子形成2个单键,钠离子与Xm-形成离子键。
(a-xb),a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数,1,3,5,6代表氧原子,2,4代表B原子,2号B形成3个键,则B原子为sp2杂化,4号B形成4个键,则B原子为sp3杂化;3号氧原子形成2个单键,钠离子与Xm-形成离子键。

【题目】毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl22H2O的流程如下:
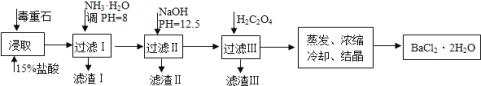
(1)写出“浸取”环节发生的主要离子方程式______。实验室用37%的盐酸配置15%的盐酸,除量筒外还需使用下列仪器中的______。(双选,填选项字母)
a.烧杯b.容量瓶c.滴定管d.玻璃棒
(2)下图是一些难溶氢氧化物在不同pH下的沉淀一溶解图
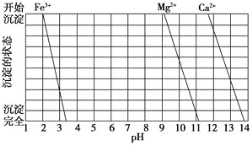
已知:Ksp(BaC2O4)= 1.6×10-7, Ksp(CaC2O4)= 2.3×10-9,
①滤渣I中含_____(填化学式)。再加入NaOH调节pH=12.5可除去______(填离子符号)
②加入H2C2O4应避免过量的原因是________
(3)25℃,H2C2O4的电离平衡常数如下:
H2C2O4 | Ka1=5.36×10-2 | Ka2=5.35×10-5 |
①HC2O4-的电离平衡常数表达式Ka2=__________
②NaHC2O4溶液呈_______(酸性、碱性、中性)