题目内容
【题目】常温下,用![]() 溶液,分别滴定
溶液,分别滴定![]() 浓度均为
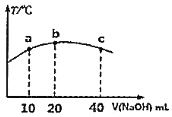
浓度均为![]() 溶液和HCN溶液,所得滴定曲线如图。下列说法正确的是
溶液和HCN溶液,所得滴定曲线如图。下列说法正确的是![]()

A.点![]() 和点
和点![]() 所示溶液中:
所示溶液中:![]()
B.醋酸的滴定终点是![]()
C.滴定![]() 过程中不可能出现:
过程中不可能出现:![]()
D.滴定HCN过程中可以用酚酞试液指示终点
【答案】A
【解析】
根据图知,相同浓度的HCN和![]() 溶液中,pH:
溶液中,pH:![]() ,说明
,说明![]() 酸性大于HCN,分别加入20mLNaOH溶液时,其溶质分别是NaCN和HCN、
酸性大于HCN,分别加入20mLNaOH溶液时,其溶质分别是NaCN和HCN、![]() 和
和![]() 且物质的量浓度相等;
且物质的量浓度相等;
A. 任何电解质溶液中都存在物料守恒,点![]() 和点
和点![]() 所示溶液中,根据物料守恒得
所示溶液中,根据物料守恒得![]() ,
,![]() ,则
,则![]() ,所以得
,所以得![]() ,故A正确;
,故A正确;
B. 理论上,滴定终点时,醋酸与氢氧化钠恰好反应生成醋酸钠,溶液显碱性,而![]() 处,溶液显中性,说明醋酸稍微过量,故B错误;
处,溶液显中性,说明醋酸稍微过量,故B错误;
C. 当刚刚开始滴定时,加入的氢氧化钠很少,溶液显酸性,溶液中醋酸分子的浓度最大,此时溶液中离子浓度关系为:![]() ,故C错误;
,故C错误;
D. 当加入20mLNaOH溶液时,其溶质是等物质的量浓度的NaCN和HCN,此时溶液的pH在![]() 之间,即只有一半HCN参加反应时,已达到酚酞的变色范围,所以不能用酚酞试液指示终点,故D错误;
之间,即只有一半HCN参加反应时,已达到酚酞的变色范围,所以不能用酚酞试液指示终点,故D错误;
答案选A。

 智慧小复习系列答案
智慧小复习系列答案【题目】下表列出了①~⑩十种元素在周期表中的位置。
族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ④ | ⑩ | |||||
3 | ⑤ | ⑥ | ⑦ | ③ | ⑧ | ⑨ | ||
回答下列问题:
(1)①、④按原子个数比1:1 组成的分子的电子式为____________________ ;由②、④两种元素组成的一种无毒化合物的结构式为 _____________________。
(2)这10种元素中,化学性质最不活泼的元素是_____________(填元素符号,下同),得电子能力最强的原子是__________________,失电子能力最强的单质与水反应的化学方程式是_________________________。
(3)用化学方程式表示②和⑨两种元素的非金属性强弱:________________________ 。
(4)元素③的气态氢化物和元素⑧的气态氢化物中,易于制备的是 ____________________(填化学式)
(5)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应,其离子方程式为 ______________________________。
(6)元素 ①、④、⑤两两之间可以形成两种类型的化合物,写出一种共价化合物的化学式:___________________ ;写出一种离子化合物的化学式:______________________。
(7)写出⑥的单质置换出②的单质的化学方程式:________________________。
【题目】几种短周期元素的原子半径及主要化合价如下表:下列叙述正确的是( )
元素代号 | X | Y | Z | W |
原子半径/pm | 160 | 143 | 70 | 66 |
主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
A.X、W元素的离子半径 W<X
B.一定条件下,W单质可以与Z元素的氢化物发生化学反应
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.一定条件下,Z单质与W的常见单质直接生成ZW2