题目内容
现有Mg、Al混合物粉末10.2克,将它溶解在500ml 4mol/L的盐酸中,若要使沉淀量达到最大值,则需要加入2mol/L NaOH溶液体积是( )
| A、500ml |
| B、1000ml |
| C、2000ml |
| D、不能确定 |
考点:有关混合物反应的计算
专题:守恒法
分析:反应过程中镁铝的转化过程分别为:Mg→MgCl2→Mg(OH)2; Al→AlCl3→Al(OH)3,Mg、Al、Mg(OH)2、Al(OH)3都不溶于水,所以沉淀质量达到最大值时溶液中的溶质是氯化钠,然后根据组成,抓住氯守恒计算.
解答:
解:根据题意知,反应过程中镁铝的转化过程分别为:Mg→MgCl2→Mg(OH)2; Al→AlCl3→Al(OH)3;
Mg、Al、Mg(OH)2、Al(OH)3都不溶于水,所以沉淀质量达到最大值时溶液中的溶质是氯化钠,
根据n( NaOH)=n(HCl)计算,
设加入2mol/L的氢氧化钠溶液的体积为xL,2mol/L×xL=0.5L×4mol/L,x=1
所以需加入2mol/L的氢氧化钠溶液的体积为1L即1000mL.
故选B.
Mg、Al、Mg(OH)2、Al(OH)3都不溶于水,所以沉淀质量达到最大值时溶液中的溶质是氯化钠,
根据n( NaOH)=n(HCl)计算,
设加入2mol/L的氢氧化钠溶液的体积为xL,2mol/L×xL=0.5L×4mol/L,x=1
所以需加入2mol/L的氢氧化钠溶液的体积为1L即1000mL.
故选B.
点评:本题考查了镁铝及其化合物的性质,知道沉淀的质量达最大时溶液中的溶质成分是解本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列反应的离子方程式书写正确的是( )
| A、硫酸铜溶液中加过量的氨水:Cu2++2NH3?H2O═Cu(OH)2↓+2NH4+ |
| B、用食醋检验牙膏中碳酸钙的存在:CaCO3+2H+═Ca2++CO2↑+H2O |
| C、用碘化钾淀粉溶液检验亚硝酸钠中NO2-的存在:NO2-+2I-+2H+═NO↑+I2+H2O |
| D、向硫酸铝铵[NH4Al(SO4)2]溶液中滴加足量Ba(OH)2溶液NH4++Al3++2SO42-+2Ba2++5OH-=AlO2-+2BaSO4↓+NH3?H2O+2H2O |
下列反应中必须加入氧化剂才能进行的是( )
| A、Cl2→Cl- |
| B、Zn→Zn2+ |
| C、KClO3→KCl |
| D、CuO→CuCl2 |
能正确表示下列化学反应的离子方程式的是( )
| A、氢氧化钡溶液与硫酸的反应 OH-+H+=H2O |
| B、金属钠与水反应 Na+H2O=Na++OH-+H2↑ |
| C、铜片插入硝酸银溶液中 Cu+Ag+=Cu2++Ag |
| D、碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2↑ |
物质的量相同的N2、O2、CO2混合后,通过Na2O2颗粒一段时间,测得体积变为原混合气体体积的
(同温同压下),此时N2、O2、CO2的物质的量之比为( )
| 8 |
| 9 |
| A、1:1:0 |
| B、6:9:0 |
| C、3:4:1 |
| D、3:3:2 |
下列依据相关实验得出的结论正确的是( )
| A、向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定是碳酸盐溶液 |
| B、用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定含有Na+ |
| C、将某气体通入溴水中,溴水颜色褪去,该气体一定是乙烯 |
| D、向某溶液中滴加KSCN 溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+ |
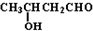

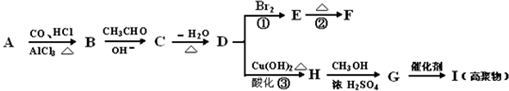


 多巴胺是一种神经递质,用来帮助细胞传送脉冲的化学物质.这种脑内分泌物主要负责大脑的情感,将兴奋及开心的信息传递,使人感到愉悦和快乐.多巴胺可由香兰素与硝基甲烷缩合,再经锌还原水解而得,合成过程如下:
多巴胺是一种神经递质,用来帮助细胞传送脉冲的化学物质.这种脑内分泌物主要负责大脑的情感,将兴奋及开心的信息传递,使人感到愉悦和快乐.多巴胺可由香兰素与硝基甲烷缩合,再经锌还原水解而得,合成过程如下: