题目内容
有一包白色粉末,其中可能含有Na2CO3、NaCl、K2SO4、CuCl2、BaCl2、KCl和Na2SO4,现按下列步骤进行实验:
(1)将该粉末溶于水得无色溶液和白色沉淀
(2)在滤出的沉淀中加入稀HNO3后,沉淀完全溶解,同时产生无色气体
(3)取滤液做焰色反应,火焰呈黄色,隔着蓝色钴玻璃观察,火焰呈紫色.
由上述实验现象推断:混合物中一定含有 ;一定不含 ;不能肯定是否含有 .
(1)将该粉末溶于水得无色溶液和白色沉淀
(2)在滤出的沉淀中加入稀HNO3后,沉淀完全溶解,同时产生无色气体
(3)取滤液做焰色反应,火焰呈黄色,隔着蓝色钴玻璃观察,火焰呈紫色.
由上述实验现象推断:混合物中一定含有
考点:几组未知物的检验
专题:
分析:根据物质的性质结合题干中的现象,通过确定存在的物质排除不能共存的物质;
依据(1)可知一定无CuCl2,一定有BaCl2;可能存在含碳酸根或硫酸根的物质;
依据(2)判断沉淀一定有碳酸钡,无硫酸钡;
依据(3)确定有钠元素,一定有钾元素;氯离子的检验方法分析氯化钠的存在.
依据(1)可知一定无CuCl2,一定有BaCl2;可能存在含碳酸根或硫酸根的物质;
依据(2)判断沉淀一定有碳酸钡,无硫酸钡;
依据(3)确定有钠元素,一定有钾元素;氯离子的检验方法分析氯化钠的存在.
解答:
解:(1)将该粉末溶于水得无色溶液和白色沉淀,可判断一定无CuCl2,一定有BaCl2,因为只有钡离子才可以形成沉淀,同时可能含碳酸根的化合物或含硫酸根离子的化合物;
(2)在滤出的沉淀中加入稀硝酸,沉淀全部溶解,同时产生无色气体,说明沉淀一定有碳酸钡,一定没有硫酸钡,反应为:Ba2++CO32-=BaCO3↓,BaCO3+2H+=Ba2++CO2↑+H2O;
(3)取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,见到有紫色火焰,说明一定有钠离子和钾离子,所以原混合物中一定含有Na2CO3和KCl;综上所述:原混合物中一定含有Na2CO3、KCl、BaCl2;一定不含有CuCl2、K2SO4、Na2SO4,可能含有NaCl,
故答案为:Na2CO3、KCl、BaCl2;CuCl2、K2SO4、Na2SO4;NaCl.
(2)在滤出的沉淀中加入稀硝酸,沉淀全部溶解,同时产生无色气体,说明沉淀一定有碳酸钡,一定没有硫酸钡,反应为:Ba2++CO32-=BaCO3↓,BaCO3+2H+=Ba2++CO2↑+H2O;
(3)取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,见到有紫色火焰,说明一定有钠离子和钾离子,所以原混合物中一定含有Na2CO3和KCl;综上所述:原混合物中一定含有Na2CO3、KCl、BaCl2;一定不含有CuCl2、K2SO4、Na2SO4,可能含有NaCl,
故答案为:Na2CO3、KCl、BaCl2;CuCl2、K2SO4、Na2SO4;NaCl.
点评:本题考查了物质检验的方法和应用,关键是依据实验现象做出判断,利用存在的物质排除不存在的物质,属于常考题.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
下列离子方程式书写正确的是( )
| A、将过量的CO2通入Ca(ClO)2溶液中:H2O+CO2+Ca2++2ClO-=CaCO3↓+2HClO |
| B、将少量NaOH溶液加入到NH4HCO3溶液中:OH-+HCO3-=CO32-+H2O |
| C、Fe3O4与稀HNO3反应:Fe3O4+8H+=Fe2++2Fe3++4H2O |
| D、向NaHCO3溶液中加入少量Ca(OH)2:HCO3-+Ca2++OH-=CaCO3↓+H2O |
下列离子方程式中,不正确的是( )
| A、向FeCl2溶液中通入Cl22Fe2++Cl2=2Fe3++2Clˉ |
| B、FeCl3溶液跟过量氨水 Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+ |
| C、碳酸氢钙溶液跟稀硝酸 Ca(HCO3)2+2H+=Ca2++2H2O+2CO2↑ |
| D、钠与水的反应 2Na+2H2O=2Na++2OH-+H2↑ |
已知反应2NO2(g)+O3(g)?N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图象作出判断正确的是( )
A、 升高温度,平衡常数减小 |
B、 0~3内,反应速率为v(NO2)=0.2mol?L-1 |
C、 t1时仅加入催化剂,平衡正向移动 |
D、 达平衡时,仅改变x,则x为c(O2) |
固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体的最外电子层结构,则下列有关说法不正确的是( )
| A、1 mol NH5中含有5 NA个N-H键(NA表示阿伏加德罗常数) |
| B、NH5中既有共价键又有离子键 |
C、NH5的电子式为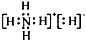 |
| D、它与水反应的离子方程式为NH4++H-+H2O=NH3?H2O+H2↑ |
 某研究性学习小组的同学在实验室对Cl2使有色物质褪色的机理进行了探究.
某研究性学习小组的同学在实验室对Cl2使有色物质褪色的机理进行了探究.