题目内容
11.ClO2是一种消毒杀菌效率高、二次污染小的水处理剂,根据世界环保联盟的要求,ClO2将逐渐取代Cl2成为生产自来水的消毒剂.工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得.有关该反应的说法正确的是( )| A. | NaClO3在反应中失去电子 | |
| B. | Na2SO3在反应中被还原为Na2SO4 | |
| C. | 在该反应中,NaClO3和Na2SO3的物质的量之比为2:1 | |
| D. | 1 mol NaClO3参加反应有2 mol 电子转移 |
分析 发生2NaClO3+Na2SO3+H2SO4=2ClO2↑+2Na2SO4+H2O,Cl元素化合价由+5价变为+4价,硫元素化合价由+4价变为+6价,得电子化合价降低的反应物是氧化剂,失电子化合价升高的反应物是还原剂,氧化剂被还原,还原剂被氧化,以此来解答.
解答 解:A.Cl元素的化合价降低,则NaClO3在反应中得到电子,故A错误;
B.Na2SO3在反应中失去电子被氧化为Na2SO4,故B错误;
C.由2NaClO3+Na2SO3+H2SO4=2ClO2↑+2Na2SO4+H2O可知,NaClO3和Na2SO3的物质的量之比为2:1,故C正确;
D.1 mol NaClO3参加反应有1 mol×(5-4)=1mol电子转移,故D错误;
故选C.
点评 本题考查氧化还原反应,为高频考点,把握发生的反应及元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意基本概念的应用及元素化合价判断,题目难度不大.

练习册系列答案
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目
1.在一定条件下,动植物油脂与醇反应可制备生物柴油,化学方程式如下:
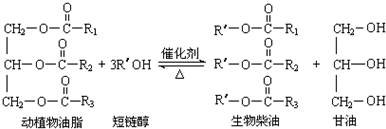
下列叙述正确的是( )

下列叙述正确的是( )
| A. | “地沟油”可用于制备生物柴油 | B. | 生物柴油属于油脂 | ||
| C. | 该反应属于酯化反应 | D. | 生物柴油的氧化反应是吸热反应 |
2.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温常压下,8g CH4含有4NA个氢原子 | |
| B. | 1 mol Cu与足量FeCl3溶液反应,转移2NA个电子 | |
| C. | 1L 0.1 mol/L (NH4)2SO4溶液中含有0.2NA个NH4+ | |
| D. | 10 L pH=l 的硫酸溶液中含有的H+离子数为2NA |
19.下列烷烃进行一氯取代后,只能生成三种沸点不同的产物的是( )
| A. | CH3CH2CH3 | B. | CH3CH3 | ||
| C. | CH3C H2CH2 CH2CH3 | D. | CH3C H2CH2CH3 |
6.碘具有多种放射性同位素.131 53I俗称“碘131”,广泛地用于医学诊断作为追踪剂和甲状腺内分泌失调症的治疗.下列有关131 53I叙述正确的是( )
| A. | 碘元素的相对原子质量为131 | |
| B. | 131 53I是一种新发现的碘的核素 | |
| C. | 131 53I位于元素周期表中第4周期ⅦA族 | |
| D. | 131 53I核内的中子数与核外电子数之差为29 |
16.下列关于元素周期表的说法正确的是( )
| A. | 18个纵行代表18个族 | |
| B. | 短周期共有32种元素 | |
| C. | 元素周期表共有七个横行代表七个周期 | |
| D. | 第IA族全部是金属元素 |
3.下列叙述正确的是( )
| A. | 40 K和40 Ca原子中的质子数和中子数都相等 | |
| B. | 某元素最外层只有一个电子,则它一定是金属元素 | |
| C. | 任何原子或离子的组成中都含有质子 | |
| D. | 同位素的不同核素物理、化学性质完全相同 |
1.化学反应可视为旧键断裂和新键形成的过程.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ•mol-1):P-P:198P-O:360O═O:498,则生成1mol P4O6该反应P4(白磷)+3O2═P4O6中的能量变化为( )


| A. | 吸收1638 kJ能量 | B. | 放出1638 kJ能量 | C. | 吸收126 kJ能量 | D. | 放出126 kJ能量 |
 量取16.0mL 10.0mol•L-1HCl溶液,加蒸馏水稀释至100mL,取两份稀释后的HCl溶液各25mL,分别加入等质量的Mg和Al,相同条件下充分反应,产生氢气的体积随时间变化的曲线如图所示(氢气体积已折算成标准状况下的体积),请计算:
量取16.0mL 10.0mol•L-1HCl溶液,加蒸馏水稀释至100mL,取两份稀释后的HCl溶液各25mL,分别加入等质量的Mg和Al,相同条件下充分反应,产生氢气的体积随时间变化的曲线如图所示(氢气体积已折算成标准状况下的体积),请计算: