题目内容
2.下列各组物质只用胶头滴管和试管就能鉴别的是( )| A. | KOH溶液与AlCl3溶液 | B. | AlCl3溶液与氨水 | ||
| C. | NaAlO2溶液与盐酸 | D. | NaHCO3溶液与盐酸 |
分析 只要用试管和胶头滴管,不用任何化学试剂就可以鉴别的物质可以采用相互滴加的方法检验,滴加顺序不同,现象不同的可以鉴别,否则不能鉴别,以此进行解答.
解答 解:A.将氯化铝溶液滴加到KOH溶液中先没有现象,后生成沉淀,将KOH滴到氯化铝溶液中先生成沉淀后沉淀消失,二者现象不同,可鉴别,故A正确;
B.无论将氨水滴到氯化铝溶液中还是将氯化铝溶液滴到氨水中都生成白色沉淀,现象相同,不能鉴别,故B错误;
C.向NaAlO2溶液加盐酸,先有沉淀后沉淀消失,而向盐酸中加NaAlO2溶液,先没有沉淀后生成沉淀,现象不同,能鉴别,故C正确;
D.NaHCO3溶液滴入稀盐酸中和将盐酸滴入NaHCO3溶液中,都会立刻生成气体,反应现象相同,无法鉴别,故D错误;
故选AC.
点评 本题考查利用滴加顺序不同鉴别物质,为高频考点,题目难度中等,明确常见元素单质及其化合物的性质为解答关键,注意掌握物质检验与鉴别方案的设计与评价原则,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
8.化学与人类生产、生活、环境保护及社会可持续发展密切相关,下列有关叙述正确的是( )
| A. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| B. | PM2.5表面积大,能吸附大量的有毒有害物质,对人的肺功能造成很大危害 | |
| C. | 二氧化硅广泛应用于太阳能电池、计算机芯片 | |
| D. | 汽车尾气中含有大量大气污染物,这是汽油不完全燃烧造成的 |
9.已知几种共价键能数据如下:
(1)通过计算,写出合成氨反应的热化学方程式:N2(g)+3H2(g)?2NH3(g)△H=-90.8kJ/mol.
(2)某温度下,以0.1mol N2和0.4mol H2作为初始反应物,在体积为2L的恒容密闭容器中进行合成氨反应,5min后测得反应放热2270J.则此时容器中N2的物质的量浓度c(N2)=0.0375mol/L,用H2表示的化学反应速率v(H2)=0.0075mol•L-1min-1.
| 共价键 | N≡N | H-H | N-H |
| 键能(kJ/mol) | 946 | 436 | 390.8 |
(2)某温度下,以0.1mol N2和0.4mol H2作为初始反应物,在体积为2L的恒容密闭容器中进行合成氨反应,5min后测得反应放热2270J.则此时容器中N2的物质的量浓度c(N2)=0.0375mol/L,用H2表示的化学反应速率v(H2)=0.0075mol•L-1min-1.
14.化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法错误的是( )
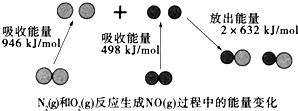

| A. | 该反应的热化学方程式为:N2(g)+O2(g)═2NO(g)△H=+180kJ•mol-1 | |
| B. | 1mol N2(l)和NA个O2(l)反应生成2mol NO(g)时,吸收的能量为180kJ | |
| C. | 1mol N2(g)和1mol O2(g)具有的总能量小于2mol NO(g)具有的总能量 | |
| D. | 通常情况下,N2(g)和O2(g)混合不能直接生成NO(g) |
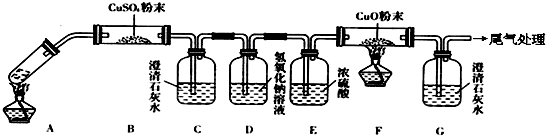
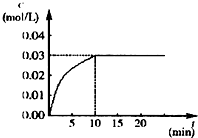 在某一容积为5L的密闭容器内,加入 0.2mol的CO和0.2mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),△H<0,反应中CO2的浓度随时间变化情况如图:
在某一容积为5L的密闭容器内,加入 0.2mol的CO和0.2mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),△H<0,反应中CO2的浓度随时间变化情况如图: