题目内容
11.想一想:Ba(OH)2(固体)、CuSO4(固体)、CH3COOH(液体)这些物质为什么归为一类,下列哪些物质还可以和它们归为一类( )①75%的酒精溶液 ②硝酸钠 ③碱石灰 ④豆浆.
| A. | ①④ | B. | ② | C. | ②③ | D. | ③④ |
分析 混合物是两种或两种以上的物质组成,纯净物是单一的一种物质,由同种分子构成的物质是纯净物,由不同种分子构成的物质是混合物.
解答 解:混合物是两种或两种以上的物质组成,纯净物是单一的一种物质,由同种分子构成的物质是纯净物,由不同种分子构成的物质是混合物.
Ba(OH)2(固体)、CuSO4(固体)、纯醋酸(液态)都只含有一种物质,是纯净物.
①.75%的酒精溶液是乙醇和水的混合物,故①错误;
②、硝酸钠是纯净物,故②正确;
③.碱石灰是混合物,故③错误;
④.豆浆是蛋白质,水等的混合物,故④错误.
故选B.
点评 本题考查混合物纯净物的概念,注意对概念的理解和区分,正确从宏观组成和微观构成两个角度来把握,还要注意特殊情况,比如碳单质和金属单质及稀有气体都是又原子直接构成的,题目较简单.

练习册系列答案
相关题目
17.下列叙述正确的是( )
| A. | AlCl3溶液和Al2(SO4)3溶液加热、蒸发、浓缩、结晶、灼烧,所得固体的成分相同 | |
| B. | 配制FeCl3溶液时,将FeCl3固体溶解在硫酸中,然后再用水稀释到所需的浓度 | |
| C. | 铁锅生锈的正极反应为:O2+2H2O+4e-═4OH- | |
| D. | 工业上电解饱和食盐水的阳极反应为:2H++2e-═H2↑ |
2.下列各组物质只用胶头滴管和试管就能鉴别的是( )
| A. | KOH溶液与AlCl3溶液 | B. | AlCl3溶液与氨水 | ||
| C. | NaAlO2溶液与盐酸 | D. | NaHCO3溶液与盐酸 |
19.下列说法错误的是( )
| A. | H2SO4、HClO、BaCO3是电解质 | |
| B. | 生石灰与水混合发生化学、物理变化 | |
| C. | 丁达尔效应可以区分溶液与胶体 | |
| D. | 光导纤维中所用材料为晶体硅 |
6.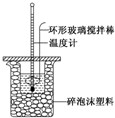 某实验小组用0.50mol•L-1 NaOH溶液和0.50mol•L-1 硫酸溶液进行反应热的测定,实验装置如图所示.
某实验小组用0.50mol•L-1 NaOH溶液和0.50mol•L-1 硫酸溶液进行反应热的测定,实验装置如图所示.
(1)写出该反应的热化学方程式生成1mol H2O(l)时的反应热为-57.3kJ•mol-1$\frac{1}{2}$H2SO4(aq)+NaOH(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3 kJ•mol-1.
(2)取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如表所示.
①近似认为0.50mol•L-1 NaOH溶液和0.50mol•L-1 硫酸溶液的密度都是1.0g•mL-1,中和后生成溶液的比热容c=4.18J•g-1•℃-1.则生成1mol H2O(l)时的反应热△H=-53.5kJ/mol(取小数点后一位).
②上述实验数值结果与-57.3kJ•mol-1有偏差,产生偏差的原因不可能是(填字母)b.
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(3)若将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1L 1mol•L-1 的稀盐酸恰好完全反应,其反应热分别为△H1、△H2、△H3,则△H1、△H2、△H3的大小关系为△H1=△H2<△H3;.
 某实验小组用0.50mol•L-1 NaOH溶液和0.50mol•L-1 硫酸溶液进行反应热的测定,实验装置如图所示.
某实验小组用0.50mol•L-1 NaOH溶液和0.50mol•L-1 硫酸溶液进行反应热的测定,实验装置如图所示.(1)写出该反应的热化学方程式生成1mol H2O(l)时的反应热为-57.3kJ•mol-1$\frac{1}{2}$H2SO4(aq)+NaOH(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3 kJ•mol-1.
(2)取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如表所示.
| 温度 次数 | 起始温度t1/℃ | 终止温 度t2/℃ | 温度差 平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②上述实验数值结果与-57.3kJ•mol-1有偏差,产生偏差的原因不可能是(填字母)b.
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(3)若将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1L 1mol•L-1 的稀盐酸恰好完全反应,其反应热分别为△H1、△H2、△H3,则△H1、△H2、△H3的大小关系为△H1=△H2<△H3;.
20.下列实验操作或装置(略去部分夹持仪器)正确的是( )
| A. | 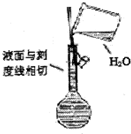 配制溶液 | B. | 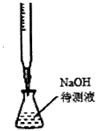 中和滴定 | ||
| C. | 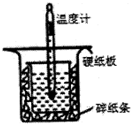 测定中和反应的反应热 | D. | 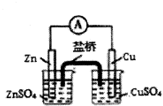 构成铜锌原电池 |
1.下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语回答下列问题:
(1)⑥的最低负价是-2;⑦的最高价含氧酸的化学式为HClO4.
(2)③、④、⑦的简单离子半径由大到小的顺序为Cl->F->Na+用离子符号表示).
(3)⑦的单质电子式为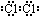 ,由②、④两种元素的原子按1:1组成化合物的电子式为
,由②、④两种元素的原子按1:1组成化合物的电子式为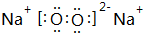 .
.
(4)②、⑥的单质中更易与①的单质反应的是氧气,用原子结构的理论解释原因是同一主族从上到下,原子半径增大,得电子能力减弱,元素的非金属减弱,所以氧气的氧化性比硫强.
(5)④、⑤的最高价氧化物对应水化物之间发生反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.
(6)若用①、②的单质和④的最高价氧化物对应水化物的溶液设计成化学电源,则该电池负极的电极反应式为H2+2OH--2e-=2H2O正极的电极反应式为O2+2H2O+4e-=4OH-.
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ||||
(2)③、④、⑦的简单离子半径由大到小的顺序为Cl->F->Na+用离子符号表示).
(3)⑦的单质电子式为
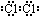 ,由②、④两种元素的原子按1:1组成化合物的电子式为
,由②、④两种元素的原子按1:1组成化合物的电子式为 .
.(4)②、⑥的单质中更易与①的单质反应的是氧气,用原子结构的理论解释原因是同一主族从上到下,原子半径增大,得电子能力减弱,元素的非金属减弱,所以氧气的氧化性比硫强.
(5)④、⑤的最高价氧化物对应水化物之间发生反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.
(6)若用①、②的单质和④的最高价氧化物对应水化物的溶液设计成化学电源,则该电池负极的电极反应式为H2+2OH--2e-=2H2O正极的电极反应式为O2+2H2O+4e-=4OH-.