题目内容
[选修2--化学与技术]
I.化学与科学、技术、社会、环境密切相关,下列做法中正确的是 (双选)
A.研制乙醇汽油(汽油中添加一定比例乙醇)技术,不能降低机动车尾气中有害气体排放
B.为了有效的发展清洁能源,采用电解水的方法大量制备H2
C.利用化学反应原理,设计和制造新的药物
D.停车场安装催化光解设施,可将汽车尾气中CO和NOx反应生成无毒气体
II.浩瀚的海洋是一个巨大的资源宝库,蕴藏着丰饶的矿产,是宝贵的化学资源,如
图是海水加工的示意图,根据下图回答问题.
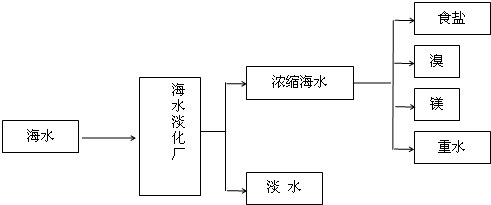
(1)海水淡化工厂通常采用的制备淡水的方法有 (写出两种).
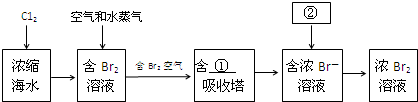
(2)如图是从浓缩海水中提取溴的流程图.写出下图中①②的化学式:① ,② ,吸收塔中发生的化学反应方程式为 .
(3)制备金属镁是通过电解熔融的MgC12,而不用MgO,其原因是 .
(4)食盐也是一种重要的化工原料,氯碱工业就是通过电解饱和食盐水来制备NaOH、H2和C12.海水中得到的粗盐中往往含有一些杂质,必须加入一些化学试剂,使杂质沉淀,处理后的盐水还需进入阳离子交换塔,其原因是 .电解食盐水在离子交换膜电解槽中进行,离子交换膜的作用是 .
(5)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4可转化为SiHCl3而循环使用.一定条件下,在20L恒容密闭容器中的反应:3SiCl4(g)+2H2(g)+Si(g)
4SiHCl3(g).达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于氯碱工业,理论上需消耗纯NaCl的质量为 kg.
I.化学与科学、技术、社会、环境密切相关,下列做法中正确的是
A.研制乙醇汽油(汽油中添加一定比例乙醇)技术,不能降低机动车尾气中有害气体排放
B.为了有效的发展清洁能源,采用电解水的方法大量制备H2
C.利用化学反应原理,设计和制造新的药物
D.停车场安装催化光解设施,可将汽车尾气中CO和NOx反应生成无毒气体
II.浩瀚的海洋是一个巨大的资源宝库,蕴藏着丰饶的矿产,是宝贵的化学资源,如
图是海水加工的示意图,根据下图回答问题.

(1)海水淡化工厂通常采用的制备淡水的方法有
(2)如图是从浓缩海水中提取溴的流程图.写出下图中①②的化学式:①

(3)制备金属镁是通过电解熔融的MgC12,而不用MgO,其原因是
(4)食盐也是一种重要的化工原料,氯碱工业就是通过电解饱和食盐水来制备NaOH、H2和C12.海水中得到的粗盐中往往含有一些杂质,必须加入一些化学试剂,使杂质沉淀,处理后的盐水还需进入阳离子交换塔,其原因是
(5)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4可转化为SiHCl3而循环使用.一定条件下,在20L恒容密闭容器中的反应:3SiCl4(g)+2H2(g)+Si(g)
| 放电 |
| 充电 |
考点:海水资源及其综合利用,硅和二氧化硅,物质分离和提纯的方法和基本操作综合应用,物质的分离、提纯和除杂
专题:化学应用
分析:Ⅰ、A、使用乙醇汽油能减少有害气体的排放,乙醇是可再生能源,
B、电解水的方法大量制备H2 ,消耗更多的能源,不经济;
C、利用化学原理可以制备新的物质;
D、CO和NOx反应在催化剂作用下反应生成氮气和二氧化碳无毒气体;
Ⅱ、(1)目前淡化海水的方法有多种,常用方法有蒸馏、电渗析以及离子交换法等,以此解答.
(2)从浓缩海水中提取溴,先进行溴离子的氧化得到溴单质,利用二氧化硫吸收溴单质富集得到溴离子,最后再次用氯气氧化;
(3)MgO的熔点为2852℃、熔点高,电解时耗能高;
(4)食盐水中含有杂质离子Mg2+、Ca2+,一定条件下生成沉淀损害离子交换膜;根据电解食盐水的产物之间能反应;
(5)利用三段分析法,根据平衡时H2与SiHCl3物质的量浓度,求出的起始物质的量,再根据2NaCl+2H2O
Cl2↑+H2↑+2NaOH,求出理论上消耗纯NaCl的质量.
B、电解水的方法大量制备H2 ,消耗更多的能源,不经济;
C、利用化学原理可以制备新的物质;
D、CO和NOx反应在催化剂作用下反应生成氮气和二氧化碳无毒气体;
Ⅱ、(1)目前淡化海水的方法有多种,常用方法有蒸馏、电渗析以及离子交换法等,以此解答.
(2)从浓缩海水中提取溴,先进行溴离子的氧化得到溴单质,利用二氧化硫吸收溴单质富集得到溴离子,最后再次用氯气氧化;
(3)MgO的熔点为2852℃、熔点高,电解时耗能高;
(4)食盐水中含有杂质离子Mg2+、Ca2+,一定条件下生成沉淀损害离子交换膜;根据电解食盐水的产物之间能反应;
(5)利用三段分析法,根据平衡时H2与SiHCl3物质的量浓度,求出的起始物质的量,再根据2NaCl+2H2O
| ||
解答:
解:(1)目前淡化海水的方法有多种,海水淡化工厂通常采用的制备淡水的方法有蒸馏法、电渗析法;
故答案为:蒸馏法、电渗析法;
(2)从浓缩海水中提取溴,先进行溴离子的氧化得到 溴单质,利用二氧化硫吸收溴单质的富集得到溴离子,最后再次用氯气氧化,吸收塔中发生的化学反应方程式为:SO2+Cl2+2H2O=H2SO4+2HCl;
故答案为:SO2;Cl2;SO2+Cl2+2H2O=H2SO4+2HCl;
(3)MgO的熔点为2852℃、熔点高,电解时耗能高,所以,工业上,电解熔融MgCl2冶炼金属镁;
故答案为:MgO的熔点为2800℃、熔点高,电解时耗能高;
(4)用试剂处理后的盐水中还含有少量Mg2+、Ca2+,碱性条件下会生成沉淀,损害离子交换膜,所以要用阳离子交换塔除去Mg2+、Ca2+;电解食盐水的产物有氯气、氢气和氢氧化钠,氯气与氢氧化钠能反应,氢气与氯气也能反应,所以电解食盐水在离子交换膜电解槽中进行;
故答案为:用试剂处理后的盐水中还含有少量Mg2+、Ca2+,碱性条件下会生成沉淀,损害离子交换膜;防止H2与C12混合发生爆炸,同时防止C1-进入阴极室,这样可以获得纯净的NaOH,;
(5)由3SiCl4(g)+2H2(g)+Si(s)?4SiHCl3(g)
起始量(mol) n 0
变化量(mol) 2x x 4x
平衡量(mol) n-2x 4x
4x=0.020mol/L×20L=0.4mol,x=0.1mol,
n-2x=0.140mol/L×20L=2.8mol,n=3.0mol,
由2NaCl+2H2O
Cl2↑+H2↑+2NaOH,
2mol 1mol
=
; m(NaCl)=350g=0.35kg;
故答案为:0.35.
故答案为:蒸馏法、电渗析法;
(2)从浓缩海水中提取溴,先进行溴离子的氧化得到 溴单质,利用二氧化硫吸收溴单质的富集得到溴离子,最后再次用氯气氧化,吸收塔中发生的化学反应方程式为:SO2+Cl2+2H2O=H2SO4+2HCl;
故答案为:SO2;Cl2;SO2+Cl2+2H2O=H2SO4+2HCl;
(3)MgO的熔点为2852℃、熔点高,电解时耗能高,所以,工业上,电解熔融MgCl2冶炼金属镁;
故答案为:MgO的熔点为2800℃、熔点高,电解时耗能高;
(4)用试剂处理后的盐水中还含有少量Mg2+、Ca2+,碱性条件下会生成沉淀,损害离子交换膜,所以要用阳离子交换塔除去Mg2+、Ca2+;电解食盐水的产物有氯气、氢气和氢氧化钠,氯气与氢氧化钠能反应,氢气与氯气也能反应,所以电解食盐水在离子交换膜电解槽中进行;
故答案为:用试剂处理后的盐水中还含有少量Mg2+、Ca2+,碱性条件下会生成沉淀,损害离子交换膜;防止H2与C12混合发生爆炸,同时防止C1-进入阴极室,这样可以获得纯净的NaOH,;
(5)由3SiCl4(g)+2H2(g)+Si(s)?4SiHCl3(g)
起始量(mol) n 0
变化量(mol) 2x x 4x
平衡量(mol) n-2x 4x
4x=0.020mol/L×20L=0.4mol,x=0.1mol,
n-2x=0.140mol/L×20L=2.8mol,n=3.0mol,
由2NaCl+2H2O
| ||
2mol 1mol
| 2×58.5g |
| 1mol |
| m(NaCl) |
| 3mol |
故答案为:0.35.
点评:本题考查了海水提取镁的过程分析,是一道综合性试题,涉及知识点比较多,要求学生有完整的知识结构和分析问题的能力,难度中等.

练习册系列答案
相关题目
下列物质中,-OH上的H最难电离的是( )
| A、CH3COOH |
| B、CH3CH2OH |
| C、H2O |
| D、C6H5OH |
下列化学变化生成物总能量比反应物总能量高的是( )
①生石灰与水反应
②铝与盐酸反应
③氯化铵与Ba(OH)2?8H20反应
④石灰石高温分解
⑤氢气与氧气反应生成H20.
①生石灰与水反应
②铝与盐酸反应
③氯化铵与Ba(OH)2?8H20反应
④石灰石高温分解
⑤氢气与氧气反应生成H20.
| A、①③④ | B、②⑨④ |
| C、②③ | D、③④ |
下列叙述正确的是( )
| A、海水中蕴含的元素有80多种,其中Mg、Br、I在海水中的总储量分别约为1.8×1015t、1×1014t、8×1010t.由于海水中镁的储量很大,工业上常以海水为原料提取镁,因此,镁元素被称为“海洋元素” | |||
B、对于可逆反应N2(g)+3H2(g)
| |||
| C、硫酸工业中,从吸收塔上部导出的气体再次通入接触室进行二次氧化,进一步吸收后,二氧化硫的含量很少,可直接排放到空气中 | |||
| D、阴极射线和α-粒子散射现象都对原子结构模型的建立做出了贡献 |
 镁燃料电池具有高比能量、安全和成本低等特点,在军事和民用方面有良好的应用前景.镁燃料电池的氧化剂可以利用空气或者海水中的氧,还有过氧化氢和次氯酸盐等.
镁燃料电池具有高比能量、安全和成本低等特点,在军事和民用方面有良好的应用前景.镁燃料电池的氧化剂可以利用空气或者海水中的氧,还有过氧化氢和次氯酸盐等. 铝.
铝. 如图是实验室制取 氯气的实验装置.
如图是实验室制取 氯气的实验装置.