题目内容
2.已知H++OH-═H2O生成1mol H2O放出热量57.3kJ,下列反应中能放出57.3kJ热量的是( )| A. | 稀硫酸与Ba(OH)2溶液反应生成1 mol水 | |
| B. | 稀盐酸与氨水反应生成1 mol H2O | |
| C. | 1 mol稀H2SO4与足量NaOH溶液反应 | |
| D. | 稀盐酸与稀Ba(OH)2溶液反应生成1 mol水 |
分析 A、稀硫酸与Ba(OH)2溶液反应生成硫酸钡沉淀和水;
B、一水合氨是弱碱,电离过程需要吸热;
C、1mol稀H2SO4与足量NaOH溶液反应会生成2mol的水;
D、稀盐酸与Ba(OH)2溶液反应生成1mol水的实质是:H++OH-=H2O.
解答 解:A、稀硫酸与Ba(OH)2溶液反应生成1 mol水的同时又生成硫酸钡沉淀,则放出的热量大于57.3KJ,故A错误;
B、一水合氨是弱碱,电离过程需要吸热,稀盐酸与氨水反应生成1molH2O放出的热量会小于57.3KJ,故B错误;
C、1mol稀H2SO4与足量NaOH溶液反应会生成2mol的水,放出热量114.6KJ,故C错误;
D、稀盐酸与稀Ba(OH)2溶液反应生成1mol水的实质是:H++OH-=H2O,放出的热量是57.3KJ,故D正确;
故选D.
点评 本题考查学生中和热的含义:强酸和强碱的稀溶液反应生成1mol水所放出的热量成为中和热.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
1.下列各物质中所含有的分子数最多的是( )
| A. | 标准状况下11.2L氯气 | B. | 17g氨气(NH3) | ||
| C. | 0.8mol氧气 | D. | 1.204×1024个H2O分子 |
13.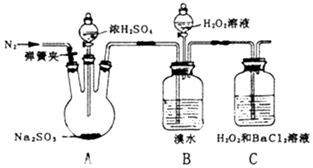 为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验).
为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验).
(1)A中发生反应的化学方程式是Na2SO3(固)+H2SO4(浓)=Na2SO4+SO2↑+H2O.
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性:H2O2>SO2.
①乙同学认为不能得出此结论,认为在滴加浓硫酸之前应增加一步操作,该操作是打开弹簧夹,通入N2,待排净装置内空气后,关闭弹簧夹.
②丙同学认为还应该在B和C之间增加洗气瓶D,D中盛放的试剂是CCl4或苯或饱和NaHSO3溶液.
(3)iii中滴入少量H2O2没有明显变化.提出假设:
观点1:H2O2的量少不能氧化Br-
观点2:B中有未反应的H2SO3
为验证观点2,应进行的实验操作及现象是取少量滴加H2O2溶液前的B中溶液于试管中,加热,将气体通入品红溶液中,品红溶液褪色.
(4)通过上述全部实验,得出结论:H2O2、SO2、Br2氧化性由强到弱的顺序是H2O2>Br2>SO2.
 为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验).
为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验).| 实验操作 | 实验现象 |
| i.打开A中分液漏斗活塞,滴加浓硫酸 | A中有气泡产生,B中红棕色溴水褪色,C中有白色沉淀 |
| ii.取C中沉淀加入盐酸 | C中白色沉淀不溶解 |
| iii.打开B中分液漏斗活塞,逐滴滴加H2O2 | 开始时颜色无明显变化,继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性:H2O2>SO2.
①乙同学认为不能得出此结论,认为在滴加浓硫酸之前应增加一步操作,该操作是打开弹簧夹,通入N2,待排净装置内空气后,关闭弹簧夹.
②丙同学认为还应该在B和C之间增加洗气瓶D,D中盛放的试剂是CCl4或苯或饱和NaHSO3溶液.
(3)iii中滴入少量H2O2没有明显变化.提出假设:
观点1:H2O2的量少不能氧化Br-
观点2:B中有未反应的H2SO3
为验证观点2,应进行的实验操作及现象是取少量滴加H2O2溶液前的B中溶液于试管中,加热,将气体通入品红溶液中,品红溶液褪色.
(4)通过上述全部实验,得出结论:H2O2、SO2、Br2氧化性由强到弱的顺序是H2O2>Br2>SO2.
17.某电动汽车配载一种可充放电的锂离子电池.放电时电池的总反应为:Li1-xCoO2+LixC6═LiCoO2+C6(x<1).下列关于该电池的说法不正确的是( )
| A. | 放电时,Li+在电解质中由正极向负极迁移 | |
| B. | 放电时,负极的电极反应式为LixC6-xe-═xLi++C6 | |
| C. | 充电时,若转移1mole-,石墨C6电极将增重7xg | |
| D. | 充电时,阳极的电极反应式为LiCoO2-xe-═Li1-xCoO2+xLi+ |
7.现有部分被氧化的Cu-Fe合金粉末8.96g,将其进行如下处理

下列说法正确的是( )

下列说法正确的是( )
| A. | 滤渣B中一定含有Cu,可能含有Fe | |
| B. | 向滤液C中滴入KSCN溶液,溶液可能变红色 | |
| C. | 合金粉末中可能含5.68gCuO | |
| D. | 气体A在标准状况下的体积为224mL |
14.下列物质的类别与所含官能团都正确的是( )
| A. |  酚-OH | B. |  羧酸-COOH | C. |  醛-CHO | D. |  CH3-O-CH3 酮 |
11.下列属于碱性氧化物的是( )
| A. | Na2O2 | B. | Fe3O4 | C. | CaO | D. | MnO(OH) |
7.NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 2.3 g Na变成Na+时,失去的电子数为0.2NA | |
| B. | 0.2NA个H2SO4与19.6 g H3PO4含有相同的氧原子数 | |
| C. | 28 g N2与CO的混合气体,所含的原子数为NA | |
| D. | 含有NA个氧原子的H2SO4的物质的量是4 mol |
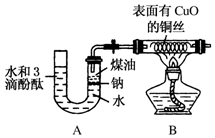 某课外活动小组为了检验钠与水反应的产物,设计如图装置(夹持装置省略).首先在U形管内加入少量煤油和几粒钠块,再从U形管高端加入水(含有酚酞),赶出空气,一会儿点燃酒精灯加热铜丝.
某课外活动小组为了检验钠与水反应的产物,设计如图装置(夹持装置省略).首先在U形管内加入少量煤油和几粒钠块,再从U形管高端加入水(含有酚酞),赶出空气,一会儿点燃酒精灯加热铜丝.