题目内容
在以Al2O3为原料制备Al(OH)3可以使用如下路线:Al2O3
AlCl3
Al(OH)3,则X最适宜用的试剂( )
| HCl |
| X |
| A、NH3?H2O |
| B、CO2 |
| C、NaOH |
| D、HCl |
考点:镁、铝的重要化合物
专题:元素及其化合物
分析:根据AlCl3制备氢氧化铝的方法来判断.
解答:
解:由AlCl3制备氢氧化铝的方法,要防止生成的氢氧化铝会不会继续溶解,又因为氢氧化铝只与强碱反应不与弱碱反应,故应该选择弱碱,故选:A
点评:主要考查氢氧化铝的制备方法的选择,抓住氢氧化铝的性质进行分析.

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案 培优三好生系列答案
培优三好生系列答案
相关题目
向盛有10mL AlCl3溶液试管,逐渐滴入加NaOH溶液的图象如图,则下列说法不正确的是( )
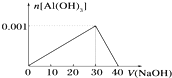

| A、AlCl3溶液的浓度为0.1mol?L-1 |
| B、NaOH溶液的浓度为0.1mol?L-1 |
| C、沉淀最大质量为0.078g |
| D、加入10mL的NaOH溶液与加入38mL的NaOH溶液产生的沉淀质量相同 |
含一个叁键的炔烃,氢化后的产物的结构简式CH3CH2CH(CH2CH3)CH2CH(CH3)CH2CH3此炔烃可能的结构有( )
| A、1种 | B、2种 | C、3种 | D、4种 |
下列事实不能用化学平衡移动原理解释的是( )
| A、合成氨工业中采用高压条件 |
| B、由H2、I2蒸气、HI组成的平衡体系加压后颜色变深 |
| C、用排饱和食盐水的方法收集Cl2 |
| D、反应CO(g)+NO2(g)═CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深 |
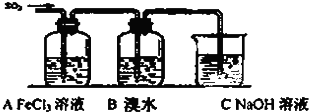
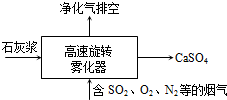 硫元素有多种化合价,可形成多种化合物.
硫元素有多种化合价,可形成多种化合物.