题目内容
(10分)聚合硫酸铁(SPFS)是一种新型的饮用水处理剂和城市污水净化剂,其化学组成可表示为[Fe2(OH)n(SO4)3 -  ]m 。某研究小组将聚合硫酸铁在一定条件下加热完全分解,对所得气体产物和固体产物进行实验探究。请利用实验室常用仪器、用品和以下试剂完成验证和探究过程(已知SO3的熔点为16.8 ℃)。
]m 。某研究小组将聚合硫酸铁在一定条件下加热完全分解,对所得气体产物和固体产物进行实验探究。请利用实验室常用仪器、用品和以下试剂完成验证和探究过程(已知SO3的熔点为16.8 ℃)。
试剂:1.0 mol·L-1的盐酸、1.0 mol·L-1的KMnO4溶液、 0.1 mol·L-1的BaCl2溶液、20%的KSCN溶液、品红溶液、蒸馏水、冰水。
(1)聚合硫酸铁中铁元素的化合价是________
(2)固体产物成分的探究
【实验设计】
实验步骤 | 现象 |
步骤1:取适量的固体产物于试管中,加入足量1.0 mol·L-1的盐酸,充分振荡使固体完全溶解。 | 固体溶解,没有观察 到气泡,溶液呈黄色 |
步骤2:取少量步骤1所得溶液于试管中,加入适量20%的KSCN溶液振荡 | 溶液呈血红色 |
步骤3:另取少量步骤1所得溶液于试管中,滴入少量1.0 mol·L-1的KMnO4溶液,振荡。 | KMnO4的紫红色不褪去 |
【思考与判断】 根据上面的信息,可以确定固体产物的成分是________;
步骤1中发生反应的离子方程式为
(3)气体产物成分的探究(不考虑水蒸气)
【提出假设】 假设1:所得气体的成分是SO3 假设2:所得气体的成分是SO2、O2
假设3:所得气体的成分是
【设计实验方案,验证假设】按下表的实验步骤写出预期现象与结论。
实验操作 | 预期现象与结论 |
步骤1:将少量气体产物通入盛有适量品红溶液的试管中,观察溶液的颜色变化,然后加热再观察溶液的颜色变化 | ①
② |
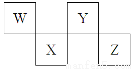
步骤2:将气体产物缓缓通过浸在冰水中的U形管(如图),然后在U形管中加入适量0.1 mol·L-1的BaCl2溶液,充分振荡 | 结合步骤1中的②
|
(1)+3 (1分)
(2)Fe2O3 (1分) Fe2O3+6H+= 2Fe3++3H2O (2分)
(3)SO3、SO2、O2 (2分)
实验操作 | 预期现象与结论 |
| ①若品红溶液不褪色,则假设1成立 (1分) ②若品红溶液褪色,加热后又恢复红色,则假设2或3成立 (1分) |
| 结合步骤1中的②: ①若无白色沉淀生成,则假设2成立 (1分) ②若有白色沉淀生成,则假设3成立 (1分) |
【解析】
试题分析:(1)在任何化合物中所有元素正负化合价代数和为0,由于聚合硫酸铁化学式是[Fe2(OH)n(SO4)3 - ]m,所以其中铁元素的化合价是[2×(3- )+n]÷2=+3;(2)固体完全溶解在盐酸中,没有观察到气泡,溶液呈黄色,则固态是Fe2O3;在步骤1中Fe2O3与盐酸发生反应的离子方程式为Fe2O3+6H+= 2Fe3++3H2O;(3)根据题意可知:假设3:所得气体的成分是SO3、SO2、O2;步骤1:将少量气体产物通入盛有适量品红溶液的试管中,观察溶液的颜色变化,然后加热再观察溶液的颜色变化,①若品红溶液不褪色,则假设1成立;②若品红溶液褪色,加热后又恢复红色,则假设2或3成立;步骤2:将气体产物缓缓通过浸在冰水中的U形管(如图),然后在U形管中加入适量0.1 mol·L-1的BaCl2溶液,充分振荡,结合步骤1中的②:①若无白色沉淀生成,则假设2成立;②若有白色沉淀生成,则假设3成立 。
考点:考查聚合硫酸铁中Fe元素化合价的确定、分解产物的成分的确定的知识。

下表中叙述Ⅰ和叙述Ⅱ均正确并且互为因果关系的是
选项 | 叙述Ⅰ | 叙述Ⅱ |
A | NH4Cl是强酸弱碱盐 | 将NH4Cl溶液蒸干可制备NH4Cl固体 |
B | Fe3+有强氧化性 | 用KSCN溶液可以鉴别Fe3+ |
C | SO2有还原性 | 用SO2可使溴水褪色 |
D | Cl2有漂白性 | 用Cl2可与石灰乳反应制备含氯消毒剂 |
下列实验操作与预期的实验目的或结论均正确的是 ( )
选项 | 实验操作 | 预期的实验目的或结论 |
A | 对某白色固体进行焰色反应实验,火焰呈黄色 | 该物质为钠盐 |
B | SO2通入某红色溶液中,溶液褪色 | 该溶液为品红溶液 |
C | pH均为12的NaOH溶液、氨水分别用蒸馏水稀释 m倍、n倍后的pH相同 | m<n |
D | 蔗糖溶液中加入少量稀硫酸加热,然后加银氨溶液再加热 | 验证蔗糖是否发生水解 |
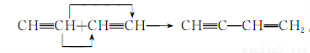 。
。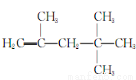 ,它是由不饱和烃乙的两个分子在一定条件下自身加成而得到的。在此反应中除生成甲外,同时还得到另一种产量更多的有机物丙,其最长的碳链仍为5个碳原子,丙是甲的同分异构体。 则乙的结构简式是___________________________________,
,它是由不饱和烃乙的两个分子在一定条件下自身加成而得到的。在此反应中除生成甲外,同时还得到另一种产量更多的有机物丙,其最长的碳链仍为5个碳原子,丙是甲的同分异构体。 则乙的结构简式是___________________________________,