题目内容
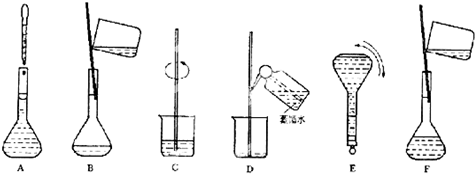
11.为达到下表中的实验目的,请选择合适的试剂及实验方法,将其标号填入对应的空格.| 实验目的 | 试剂及方法 |
| 证明地瓜中有淀粉 | B |
| 除去CO2中混有的少量CO | D |
| 检验FeCl2溶液是否变质 | C |
| 除去Na2CO3固体中NaHCO3 | A |
A.加热
B.滴加碘水
C.加入KSCN溶液
D.通过灼热的CuO.
分析 淀粉遇碘单质变蓝;
CO与CuO反应生成二氧化碳;
FeCl2溶液变质时混有铁离子,铁离子遇KSCN溶液为血红色;
NaHCO3加热分解生成碳酸钠,以此来解答.
解答 解:淀粉遇碘单质变蓝,则滴加碘水可证明,则选择B;
CO与CuO反应生成二氧化碳,则通过灼热的CuO可除杂,应选择D;
FeCl2溶液变质时混有铁离子,铁离子遇KSCN溶液为血红色,则检验是否变质可加入KSCN溶液,即选择C;
NaHCO3加热分解生成碳酸钠,则加热可除杂,即选择A,
故答案为:B;D;C;A.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
2.100mL 0.3mol•L-1 Na2SO4溶液和50mL 0.2mol•L-1 Al2(SO4)3溶液混合后(混合后溶液体积变化忽略不计),溶液中SO${\;}_{4}^{2-}$的物质的量浓度为( )
| A. | 0.40mol•L-1 | B. | 0.50mol•L-1 | C. | 0.20 mol•L-1 | D. | 0.25 mol•L-1 |
19.下列对人体健康无害的是( )
| A. | 用工业石蜡给瓜子美容 | B. | 用工业酒精(含甲醇)配兑饮用酒 | ||
| C. | 食用加碘盐预防碘缺乏病 | D. | 食用亚硝酸盐超标的腊肉 |
6.四个体积相同的密闭容器中,在一定条件下,发生如下反应:N2+3H2$?_{催化剂}^{高温、高压}$2NH3,化学反应速率最小的是( )
| 容器 | 温度(℃) | N2(mol) | H2(mol) | 催化剂 |
| A | 500 | 1 | 3 | 有 |
| B | 500 | 0.5 | 1.5 | 有 |
| C | 450 | 1 | 3 | 无 |
| D | 450 | 0.5 | 1.5 | 无 |
| A. | A | B. | B | C. | C | D. | D |
3.有下列六种转化途径,某些反应条件和产物已略去,下列说法正确的是( )
途径①Fe$\stackrel{稀HCl}{→}$FeCl2溶液
途径②Fe$\stackrel{Cl_{2}}{→}$FeCl3$\stackrel{Fe,水}{→}$FeCl${\;}_{{\;}_{2}}$溶液
途径③Cl2$\stackrel{Na_{2}SO_{3}溶液}{→}$Na2SO4溶液
途径④Cl2$\stackrel{NaOH溶液}{→}$NaClO溶液$\stackrel{Na_{2}SO_{3}溶液}{→}$Na2SO4溶液
途径⑤S$\stackrel{浓HNO_{3}}{→}$H2SO4
途径⑥S$\stackrel{O_{2}}{→}$SO2$\stackrel{O_{2}}{→}$$\stackrel{H_{2}O}{→}$H2SO4.
途径①Fe$\stackrel{稀HCl}{→}$FeCl2溶液
途径②Fe$\stackrel{Cl_{2}}{→}$FeCl3$\stackrel{Fe,水}{→}$FeCl${\;}_{{\;}_{2}}$溶液
途径③Cl2$\stackrel{Na_{2}SO_{3}溶液}{→}$Na2SO4溶液
途径④Cl2$\stackrel{NaOH溶液}{→}$NaClO溶液$\stackrel{Na_{2}SO_{3}溶液}{→}$Na2SO4溶液
途径⑤S$\stackrel{浓HNO_{3}}{→}$H2SO4
途径⑥S$\stackrel{O_{2}}{→}$SO2$\stackrel{O_{2}}{→}$$\stackrel{H_{2}O}{→}$H2SO4.
| A. | 由途径①和②分别制取1mol FeCl2,理论各消耗1mol Fe,各转移2mol e- | |
| B. | 由途径③和④分别制取1mol Na2SO4,理论各消耗1mol Cl2,各转移2mol e- | |
| C. | 由途径⑤和⑥分别制取1mol H2SO4,理论各消耗1mol S,各转移6 mol e- | |
| D. | 以上说法都不正确 |
20.已知反应:
①2CH3OH(g)═CH3OCH3(g)+H2O(g)△H1=-23.9KJ•mol-1
②2CH3OH(g)═C2H4 (g)+2H2O(g)?△H2=-29.1KJ•mol-1
③CH3CH2OH(g)═CH3OCH3(g)△H3=+50.7KJ•mol-1;
在C2H4(g)+H2O(g)═CH3CH2OH(g)△H4中;△H4等于( )
①2CH3OH(g)═CH3OCH3(g)+H2O(g)△H1=-23.9KJ•mol-1
②2CH3OH(g)═C2H4 (g)+2H2O(g)?△H2=-29.1KJ•mol-1
③CH3CH2OH(g)═CH3OCH3(g)△H3=+50.7KJ•mol-1;
在C2H4(g)+H2O(g)═CH3CH2OH(g)△H4中;△H4等于( )
| A. | -48.5 KJ•mol-1 | B. | +48.5 KJ•mol-1 | C. | -45.5KJ•mol-1 | D. | +45.5 KJ•mol-1 |