题目内容
2.下列说法不正确的是( )| A. | PM2.5是指大气中直径接近于2.5×10-6m(1m=109nm)的颗粒物,也称可吸入颗粒物,这些细颗粒物分散在空气中形成的分散系是胶体 | |
| B. | 胶体的分散质粒子直径小于l00nm但大于1nm,能通过滤纸 | |
| C. | 利用丁达尔效应可以区分溶液和胶体 | |
| D. | 浊液的分散质粒子直径大于l00nm,不能通过滤纸 |
分析 胶体的分散系中分散质的直径在1~100nm,浊液的分散质粒子直径大于l00nm,溶液的分散质粒子直径小于lnm,则溶液、胶体能通过滤纸,而浊液不能通过滤纸,利用丁达尔效应可以区分溶液和胶体,据此分析.
解答 解:A.胶体的分散系中分散质的直径在1~100nm,PM2.5是指大气中直径接近于2.5×10-6m的颗粒物,直径大于100nm,则细颗粒物分散在空气中形成的分散系不是胶体,故A错误;
B.胶体的分散质粒子直径小于l00nm但大于1nm,能通过滤纸,故B正确;
C.胶体能发生丁达尔效应,而溶液不能,所以利用丁达尔效应可以区分溶液和胶体,故C正确;
D.浊液的分散质粒子直径大于l00nm,不能通过滤纸,故D正确;
故选A.
点评 本题考查胶体的性质,题目难度不大,注意PM2.5与胶体的关系来解答.

练习册系列答案
相关题目
13.下列溶液中,溶质的物质的量浓度为0.1mol/L的是( )
| A. | 将4gNaOH溶液溶入1L水中 | |
| B. | 常温下,将2.24LHCl气体溶于水配成1L溶液 | |
| C. | 含有4.9gH2SO4的溶液500mL | |
| D. | 将6.2gNa2O溶于水配成1L溶液 |
17.下列说法或表示方法正确的是( )
| A. | 若将等量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 相同条件下,1mol H2O(l)完全分解吸收的热量与H2、O2化合生成1mol H2O(l)放出的热量值不相等 | |
| C. | 在稀溶液中:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ•mol-1若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJ | |
| D. | 在101KPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l)△H=+285.8kJ/mol |
11.通常人们把拆开1mol某化学键所吸收的能量或形成1mol某化学键所释放的能量看成该化学键的键能.已知热化学方程式:N2(g)+3H2(g)=2NH3(g)△H=-92.4kJ/mol,请根据热化学方程式和表中数据计算:H-N键的键能x约为( )
| 化学键 | H-H | N≡N | H-N |
| 键能 | 436kJ/mol | 946kJ/mol | x |
| A. | 391kJ/mol | B. | 431kJ/mol | C. | 349kJ/mol | D. | 469kJ/mol |
12.下列离子反应中,表达正确的是( )
| A. | 过量的SO2通入NaOH溶液中:SO2+2OH-═SO32-+H2O | |
| B. | 用醋酸溶解CaCO3:2H+CaCO3═Ca2++H2O+CO2↑ | |
| C. | 在氯化亚铁溶液中通入氯气Fe2++Cl2═Fe3++2Cl- | |
| D. | NaHCO3溶液中加入过量的Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O |
 向一容积为5L的恒容密闭容器内,充入0.2mol CO和0.4mol H2O,在一定条件下发生反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H>0.反应中CO2的浓度(c) 随时间(t)的变化关系如图所示.
向一容积为5L的恒容密闭容器内,充入0.2mol CO和0.4mol H2O,在一定条件下发生反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H>0.反应中CO2的浓度(c) 随时间(t)的变化关系如图所示.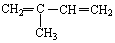 与Br2按物质的量之比1:1发生1,4加成反应方程式CH2=C(CH3)CH=CH2+Br2→CH2BrC(CH3)=CHCH2Br
与Br2按物质的量之比1:1发生1,4加成反应方程式CH2=C(CH3)CH=CH2+Br2→CH2BrC(CH3)=CHCH2Br