题目内容
6.下列说法错误的是( )| A. | 铍、镁、钙、锶、钡等碱土金属元素,在自然界都以化合态存在 | |
| B. | 从元素周期表知道,现在已经发现了113种原子 | |
| C. | 室温时,0族元素的单质都是气体 | |
| D. | 第三周期的主族元素原子的最高正价数与原子最外层电子数相等 |
分析 A、碱土金属性质较活泼,极易被氧化;
B、同一元素可能有不同的核素,元素种类不等于原子种类;
C、稀有气体常温下都是气体;
D、主族元素最高正化合价等于其主族族序数(O、F除外);
解答 解:A、碱土金属性质较活泼,极易被氧化,所以在自然界中都以化合物的形式存在,故A正确;
B、同一元素可能含有不同的核素(即原子),导致元素的种类小于原子的种类,所以发现113种元素,不等于发现113种原子,故B错误;
C、稀有气体常温下都是气体,故C正确;
D、主族元素最高正化合价等于其主族族序数(O、F除外),第三周期主族元素的最高正价数等于它所处的族序数,故D正确;
故选B.
点评 本题考查元素周期表与元素周期律,难度不大,注意掌握元素周期表中的特殊性及元素周期律.

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
16.下列物质组合中,既能和酸反应又能和碱反应的化合物是( )
①Al ②Al2O3 ③Al(OH)3 ④NaHCO3.
①Al ②Al2O3 ③Al(OH)3 ④NaHCO3.
| A. | ①②③④ | B. | ②③④ | C. | ①③④ | D. | ②③ |
14. 卤代烃在生产生活中具有广泛的应用,回答下列问题:
卤代烃在生产生活中具有广泛的应用,回答下列问题:
(1)多氯代甲烷常为有机溶剂,其分子结构为正四面体的名称为四氯甲烷;碳原子个数不大于10的烷烃分子中,其一氯代物只有一种的烷烃的个数为4个.
(2)三氟氯溴乙烷(CF3CHClBr)是一种麻醉剂,写出其所有同分异构体的结构式CHFClCF2Br、CHFBrCF2Cl、CFClBrCHF2(不考虑立体异构).
(3)聚氯乙烯是生活中常用的塑料,工业生产聚氯乙烯的一种工艺路线如下:
乙烯$→_{①}^{Cl_{2}}$1,2-二氯乙烷$→_{②}^{480-530℃}$氯乙烯$\stackrel{聚合}{→}$聚氯乙烯
反应①的反应类型为加成反应;
反应②的反应类型为消去分液.
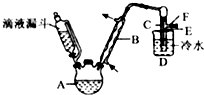
(4)实验室以乙醇、浓硫酸和溴化钠为试剂,用如图的装置制备溴乙烷,图中省去了加热装置.
有关数据见表:
①仪器B名称是球形冷凝管,仪器B的作用是冷凝回流.
②制备过程中,加入的浓硫酸必须进行稀释,其目的是AB(填序号)
A.减少副产物烯和醚的生成 B.减少Br2的生成 C.水是反应的催化剂 D.硫酸的浓度越稀反应越快
③加热应采取的方式为水浴加热;加热的目的是升高温度,加快反应速率,同时使生成的溴乙烷分离出来促进平衡右移.
④为除去收集产品中的主要杂质,应选取加入的合理试剂为Na2SO3溶液或饱和NaHSO3溶液;采用的操作是分液.
 卤代烃在生产生活中具有广泛的应用,回答下列问题:
卤代烃在生产生活中具有广泛的应用,回答下列问题:(1)多氯代甲烷常为有机溶剂,其分子结构为正四面体的名称为四氯甲烷;碳原子个数不大于10的烷烃分子中,其一氯代物只有一种的烷烃的个数为4个.
(2)三氟氯溴乙烷(CF3CHClBr)是一种麻醉剂,写出其所有同分异构体的结构式CHFClCF2Br、CHFBrCF2Cl、CFClBrCHF2(不考虑立体异构).
(3)聚氯乙烯是生活中常用的塑料,工业生产聚氯乙烯的一种工艺路线如下:
乙烯$→_{①}^{Cl_{2}}$1,2-二氯乙烷$→_{②}^{480-530℃}$氯乙烯$\stackrel{聚合}{→}$聚氯乙烯
反应①的反应类型为加成反应;
反应②的反应类型为消去分液.
(4)实验室以乙醇、浓硫酸和溴化钠为试剂,用如图的装置制备溴乙烷,图中省去了加热装置.
有关数据见表:
| 乙醇 | 溴乙烷 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 深红棕色液体 |
| 密度(g/cm3) | 0.79 | 1.44 | 3.1 |
| 沸点 | 78.5 | 38.4 | 59 |
②制备过程中,加入的浓硫酸必须进行稀释,其目的是AB(填序号)
A.减少副产物烯和醚的生成 B.减少Br2的生成 C.水是反应的催化剂 D.硫酸的浓度越稀反应越快
③加热应采取的方式为水浴加热;加热的目的是升高温度,加快反应速率,同时使生成的溴乙烷分离出来促进平衡右移.
④为除去收集产品中的主要杂质,应选取加入的合理试剂为Na2SO3溶液或饱和NaHSO3溶液;采用的操作是分液.
1.根据表中部分短周期元素的原子半径和主要化合价信息判断,以下叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.130 | 0.118 | 0.090 | 0.102 | 0.073 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 单质与同浓度稀盐酸反应的速率为L<M | |
| B. | R与T形成的化合物一定能使品红溶液褪色 | |
| C. | 氢化物的稳定性为:H2T>H2R | |
| D. | 当单质L着火时,可用CO2灭火 |
11. 含乙酸钠和对氯酚(
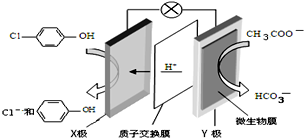
含乙酸钠和对氯酚( )的废水可以利用微生物电池除去,其原理如图所示.下列有关说法错误的是( )
)的废水可以利用微生物电池除去,其原理如图所示.下列有关说法错误的是( )
 含乙酸钠和对氯酚(
含乙酸钠和对氯酚( )的废水可以利用微生物电池除去,其原理如图所示.下列有关说法错误的是( )
)的废水可以利用微生物电池除去,其原理如图所示.下列有关说法错误的是( )| A. | Y极为该电池的负极 | |
| B. | X极的电极反应式为: +H++2e-═ +H++2e-═ +Cl- +Cl- | |
| C. | 可用硝酸酸化的硝酸银溶液验证正极产物 | |
| D. | 每处理1mol对氯酚,消耗8.2g乙酸钠 |
18.下列物质的比较正确的是( )
| A. | 酸性:HIO4>HBrO4>HClO4 | B. | 原子半径:Na>Cl>S | ||
| C. | 碱性:KOH>NaOH>LiOH | D. | 金属性:Na>Al>Mg |
15.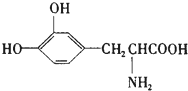 L-多巴是一种有机物,它可用于帕金森综合症的治疗,其结构简式如图:这种药物的研制是基于获得2000年诺贝尔生理学或医学奖、2001年诺贝尔化学奖的研究成果.下列关于L-多巴的叙述正确的是( )
L-多巴是一种有机物,它可用于帕金森综合症的治疗,其结构简式如图:这种药物的研制是基于获得2000年诺贝尔生理学或医学奖、2001年诺贝尔化学奖的研究成果.下列关于L-多巴的叙述正确的是( )
 L-多巴是一种有机物,它可用于帕金森综合症的治疗,其结构简式如图:这种药物的研制是基于获得2000年诺贝尔生理学或医学奖、2001年诺贝尔化学奖的研究成果.下列关于L-多巴的叙述正确的是( )
L-多巴是一种有机物,它可用于帕金森综合症的治疗,其结构简式如图:这种药物的研制是基于获得2000年诺贝尔生理学或医学奖、2001年诺贝尔化学奖的研究成果.下列关于L-多巴的叙述正确的是( )| A. | 只能与碱反应,不能与酸反应 | |
| B. | 1mol该物质最多与4molNaOH反应 | |
| C. | 该物质不能使酸性KMnO4褪色 | |
| D. | 1mol该物质最多可与1.5molHBr反应 |
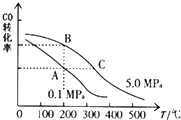 甲醇是一种可再生能源,具有开发和应用的广阔前景,请回答下列问题:
甲醇是一种可再生能源,具有开发和应用的广阔前景,请回答下列问题: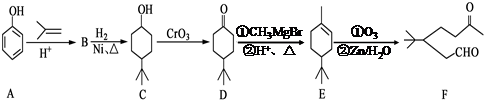
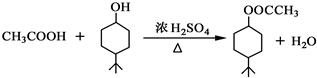 .
.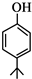 .同时满足下列条件的B的同分异构体(不包括B)共有11种:
.同时满足下列条件的B的同分异构体(不包括B)共有11种: