题目内容
下列离子方程式书写不正确的是( )
| A、往NaOH溶液中通入过量CO2:CO2+OH-=HCO3- |
| B、单质硅与烧碱溶液反应:Si+2OH-+H2O=SiO32-+2H2↑ |
| C、石英砂与烧碱反应制水玻璃:SiO2+2OH-=SiO32-+H2O |
| D、往水玻璃中通入二氧化碳:Na2SiO3+2H2O+CO2=H4SiO4↓+2Na++CO32- |
考点:离子方程式的书写
专题:
分析:A.二氧化碳过量,氢氧化钠与二氧化碳反应生成碳酸氢钠;
B.硅单质与氢氧化钠溶液反应生成硅酸钠和氢气;
C.二氧化硅为酸性氧化物,二氧化硅与氢氧化钠溶液反应生成硅酸钠和水;
D.硅酸钠为强电解质,离子方程式中硅酸钠需要拆开,不能保留化学式.
B.硅单质与氢氧化钠溶液反应生成硅酸钠和氢气;
C.二氧化硅为酸性氧化物,二氧化硅与氢氧化钠溶液反应生成硅酸钠和水;
D.硅酸钠为强电解质,离子方程式中硅酸钠需要拆开,不能保留化学式.
解答:
解:A.往NaOH溶液中通入过量CO2,反应生成碳酸氢钠,反应的离子方程式为:CO2+OH-=HCO3-,故A正确;
B.单质硅与烧碱溶液反应生成硅酸钠和氢气,反应的离子方程式为:Si+2OH-+H2O=SiO32-+2H2↑,故B正确;
C.石英砂与烧碱反应制水玻璃,二氧化硅为酸性氧化物,与氢氧化钠溶液反应生成硅酸钠,反应的离子方程式为:SiO2+2OH-=SiO32-+H2O,故C正确;
D.水玻璃中通入二氧化碳,硅酸钠在溶液中完全电离出钠离子和硅酸根离子,离子方程式中硅酸钠不能保留化学式,正确的离子方程式为:SiO32-+2H2O+CO2=H4SiO4↓+CO32-,故D错误;
故选D.
B.单质硅与烧碱溶液反应生成硅酸钠和氢气,反应的离子方程式为:Si+2OH-+H2O=SiO32-+2H2↑,故B正确;
C.石英砂与烧碱反应制水玻璃,二氧化硅为酸性氧化物,与氢氧化钠溶液反应生成硅酸钠,反应的离子方程式为:SiO2+2OH-=SiO32-+H2O,故C正确;
D.水玻璃中通入二氧化碳,硅酸钠在溶液中完全电离出钠离子和硅酸根离子,离子方程式中硅酸钠不能保留化学式,正确的离子方程式为:SiO32-+2H2O+CO2=H4SiO4↓+CO32-,故D错误;
故选D.
点评:本题考查了离子方程式的正误判断,为高考中的高频题,属于中等难度的试题,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等).

练习册系列答案
 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
乙炔的空间构型是( )
| A、正四面体 | B、平面型 |
| C、直线型 | D、三角锥形 |
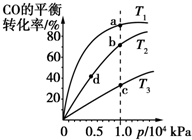 用CO合成甲醇(CH3OH)的化学反应方程式为CO(g)+2H2(g)?CH3OH(g)△H<0.按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是( )
用CO合成甲醇(CH3OH)的化学反应方程式为CO(g)+2H2(g)?CH3OH(g)△H<0.按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是( )| A、正反应速率:v(a)>v(c) v(b)>v(d) | ||||||||
| B、平衡时a点一定有n(CO):n(H2)=1:2 | ||||||||
| C、平衡常数:K(a)>K(c) K(b)=K(d) | ||||||||
D、平均摩尔质量:
|
若向略含少量水蒸气的容器中通入SO2与H2S共1mol,充分反应后,所得的氧化产物比还原产物多8g,则通入SO2和H2S的物质的量之比可能是( )
| A、1:5 | B、1:2 |
| C、2:1 | D、1:3 |
下列实验方法或操作:
①用100mL筒量配制60mL10% 的盐酸;②称量没有腐蚀性固体药品时,把药品放在托盘上称量;③浓硫酸沾到皮肤上要先用抹布擦再用大量水冲洗;④用托盘天平称取5.20gNaCl晶体;⑤蒸馏开始时应先加热在开冷凝水;⑥萃取操作时选择的萃取剂的密度不必比水大;⑦用容量瓶配制一定浓度的某溶液后,将溶液保存在容量瓶中并贴上标签.其中正确的是( )
①用100mL筒量配制60mL10% 的盐酸;②称量没有腐蚀性固体药品时,把药品放在托盘上称量;③浓硫酸沾到皮肤上要先用抹布擦再用大量水冲洗;④用托盘天平称取5.20gNaCl晶体;⑤蒸馏开始时应先加热在开冷凝水;⑥萃取操作时选择的萃取剂的密度不必比水大;⑦用容量瓶配制一定浓度的某溶液后,将溶液保存在容量瓶中并贴上标签.其中正确的是( )
| A、③⑥ | B、②③⑦ |
| C、①③⑥ | D、③⑤⑥ |
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢或锂电池的十倍,可连续使用一个月才充一次电,其电池反应为:2CH3OH+3O2H-=2CO32-+6H2O,则下列有关说法不正确的是( )
| A、放电时化学能转变为电能 |
| B、放电时CH3OH参与正极反应 |
| C、充电时阴极产CH3OH |
| D、充电时每生成1molCH3OH,则转移6mol电子 |
为了使Na2S溶液中
的比值变小,可适量加入(或通入)的物质是( )
| c(Na+) |
| c(S2-) |
| A、H2S气体 |
| B、NaOH固体 |
| C、HCl气体 |
| D、KOH固体 |
水的电离过程为H2O?H++OH-,在25℃时水的离子积为KW=1.0×10-14,在35℃时水的离子积为KW=2.1×10-14,则下列叙述正确的是( )
| A、c(H+)随着温度的升高而降低 |
| B、35℃时c(H+)>c(OH-) |
| C、35℃时的水比25℃时的水电离程度小 |
| D、水的电离是个吸热过程 |