题目内容
下列反应的离子方程式书写正确的是( )
| A、过量氯气通入溴化亚铁溶液中:3Cl2+2Fe2++4Br-═6Cl-+2Fe3++2Br2 |
| B、在硫酸铜溶液中加入过量氢氧化钡溶液:Ba2++SO42-═BaSO4↓ |
| C、次氯酸钠溶液中通入二氧化硫气体:2ClO-+SO2+H2O═2HClO+SO32- |
| D、用稀硝酸除银镜:Ag+2H++NO3-═Ag++NO2↑+H2O |
考点:离子方程式的书写
专题:
分析:A.氯气过量,溴离子、二价铁离子都被氧化;
B.漏掉铜离子与氢氧根离子的反应;
C.亚硫酸根离子能够被次氯酸根离子氧化;
D.电荷不守恒.
B.漏掉铜离子与氢氧根离子的反应;
C.亚硫酸根离子能够被次氯酸根离子氧化;
D.电荷不守恒.
解答:
解:A.过量氯气通入溴化亚铁溶液中,离子方程式:3Cl2+2Fe2++4Br-═6Cl-+2Fe3++2Br2,故A正确;
B.在硫酸铜溶液中加入过量氢氧化钡溶液,离子方程式:Cu2++2OH-+Ba2++SO42-═BaSO4↓+Cu(OH)2↓,故B错误;
C.次氯酸具有强氧化性,反应生成了硫酸根,正确反应方程式是:H2O+SO2+ClO-═SO42-+2H++Cl-,故C错误;
D.用稀硝酸除银镜,离子方程式:3Ag+4H++NO3-=3Ag++NO↑+2H2O,故D错误;
故选:A.
B.在硫酸铜溶液中加入过量氢氧化钡溶液,离子方程式:Cu2++2OH-+Ba2++SO42-═BaSO4↓+Cu(OH)2↓,故B错误;
C.次氯酸具有强氧化性,反应生成了硫酸根,正确反应方程式是:H2O+SO2+ClO-═SO42-+2H++Cl-,故C错误;
D.用稀硝酸除银镜,离子方程式:3Ag+4H++NO3-=3Ag++NO↑+2H2O,故D错误;
故选:A.
点评:本题考查了离子方程式的书写,明确离子方程式书写的方法是解题关键,注意选项A和C,反应物用量不同发生的化学反应不同.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
相同体积的氯化钠、氯化镁、氯化铝溶液分别与过量的硝酸银溶液反应,所生成的沉淀物质的量相同,则原氯化钠、氯化镁、氯化铝溶液的物质的量浓度之比为( )
| A、1:2:3 |
| B、3:2:1 |
| C、6:3:1 |
| D、6:3:2 |
设NA为阿伏加德罗常数,下列说法中正确的是( )
| A、标准状况下4.48LH2O的分子个数为2NA |
| B、22克CO2的分子个数为0.5NA |
| C、1L浓度为0.1mol/L的MgCl2溶液中Cl-为0.1NA |
| D、标准状况下2.24LNO2中原子个数为0.2NA |
下列离子方程式书写正确的是( )
| A、用铂电极电解氯化镁溶液:Cl-+2H2O═Cl2↑+H2↑+2OH- |
| B、氟气与水反应:F2+H2O═H++F-+HFO |
| C、NaHSO3溶液呈弱酸性是因为:HSO3-+H2O?SO32-+H3O+ |
| D、沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:FeCl3+3H2O═Fe(OH)3↓+3HCl |

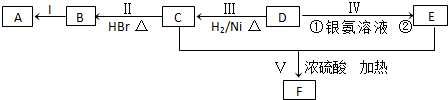

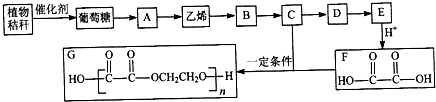
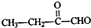 的合成路线流程图(无极试剂任用),合成路线流程图示例如下:CH3CH2OH
的合成路线流程图(无极试剂任用),合成路线流程图示例如下:CH3CH2OH