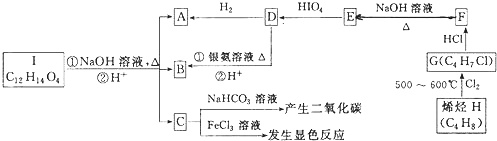
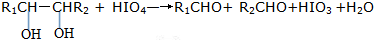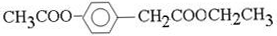题目内容
下列离子方程式书写正确的是( )
| A、用铂电极电解氯化镁溶液:Cl-+2H2O═Cl2↑+H2↑+2OH- |
| B、氟气与水反应:F2+H2O═H++F-+HFO |
| C、NaHSO3溶液呈弱酸性是因为:HSO3-+H2O?SO32-+H3O+ |
| D、沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:FeCl3+3H2O═Fe(OH)3↓+3HCl |
考点:离子方程式的书写
专题:离子反应专题
分析:A.生成氢氧化镁、氢气、氯气;
B.生成HF和氧气;
C.亚硫酸氢根离子电离大于其水解,则显酸性;
D.生成胶体,不是沉淀.
B.生成HF和氧气;
C.亚硫酸氢根离子电离大于其水解,则显酸性;
D.生成胶体,不是沉淀.
解答:
解:A.用铂电极电解氯化镁溶液的离子反应为Mg2++2Cl-+2H2O
Cl2↑+H2↑+Mg(OH)2↓,故A错误;
B.氟气与水反应的离子反应为2F2+2H2O═4HF+O2,故B错误;
C.NaHSO3溶液呈弱酸性是因为:HSO3-+H2O?SO32-+H3O+,而水解较弱,故C正确;
D.沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体的离子反应为Fe3++3H2O
Fe(OH)3(胶体)+3H+,故D错误;
故选C.
| ||
B.氟气与水反应的离子反应为2F2+2H2O═4HF+O2,故B错误;
C.NaHSO3溶液呈弱酸性是因为:HSO3-+H2O?SO32-+H3O+,而水解较弱,故C正确;
D.沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体的离子反应为Fe3++3H2O
| ||
故选C.
点评:本题考查离子反应的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重电解、水解及氧化还原反应的离子反应考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
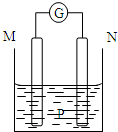 如图所示装置中,观察到电流计指针偏转;M棒变粗,N棒变细.由此判断下表中所列M、N、P物质,其中可以成立的是( )
如图所示装置中,观察到电流计指针偏转;M棒变粗,N棒变细.由此判断下表中所列M、N、P物质,其中可以成立的是( )| M | N | P | |
| A | 锌 | 铜 | 稀硫酸溶液 |
| B | 铜 | 铁 | 稀盐酸 |
| C | 银 | 锌 | 硝酸银溶液 |
| D | 锌 | 铁 | 硝酸铁溶液 |
| A、A | B、B | C、C | D、D |
下列微粒中,与OH-具有相同的质子数和相同的电子数的是( )
| A、F- |
| B、H2O |
| C、NH4+ |
| D、NH3 |
埋在地下的自来水管,在下列情况下被腐蚀的速度最慢的是( )
| A、在含有铁元素的较多的酸性土壤中 |
| B、在潮湿、疏松的土壤中 |
| C、在自来水的铁管上用导线连接一块锌片后,再埋入不透气的土壤中 |
| D、在自来水的铁管上用导线连接一块铜片后,再埋入潮湿、疏松的土壤中 |
下列说法中,正确的是( )
| A、△H>0表示放热反应,△H<0 表示吸热反应 |
| B、若反应△H>0;△S<0,则反应一定能自发进行 |
| C、1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热 |
| D、热化学方程式中的化学计量数表示物质的量,所以可以是分数 |
下列反应的离子方程式书写正确的是( )
| A、过量氯气通入溴化亚铁溶液中:3Cl2+2Fe2++4Br-═6Cl-+2Fe3++2Br2 |
| B、在硫酸铜溶液中加入过量氢氧化钡溶液:Ba2++SO42-═BaSO4↓ |
| C、次氯酸钠溶液中通入二氧化硫气体:2ClO-+SO2+H2O═2HClO+SO32- |
| D、用稀硝酸除银镜:Ag+2H++NO3-═Ag++NO2↑+H2O |
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0kJ/mol
②CH3OH(g)+
O2(g)=CO2(g)+2H2(g);△H=-192.9kJ/mol
下列说法错误的是( )
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0kJ/mol
②CH3OH(g)+
| 1 |
| 2 |
下列说法错误的是( )
| A、1mol CH3OH(g)完全燃烧放出的热量大于192.9 kJ | ||
B、根据反应①和②推知反应:H2(g)+
| ||
| C、CH3OH转变成H2的过程不一定要吸收能量 | ||
D、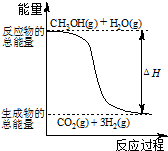 反应①中的能量变化如图所示 |
将等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生如下反应并达平衡:X(g)+Y(g)?2Z(g);△H<0.当改变某一条件并达到新平衡后,下列叙述正确的是( )
| A、升高温度,X的转化率增大 |
| B、缩小容器体积,Z的浓度不变 |
| C、保持压强不变,再充入0.1 mol X和0.1 mol Y,X的体积分数增大 |
| D、保持容器体积不变,充入一定量的氦气,Y的浓度不变 |