题目内容
7.非金属性最强的元素是( )| A. | C | B. | Si | C. | S | D. | Cl |
分析 同主族元素自上而下非金属性减弱,同周期元素自右到左非金属性减弱,据此回答.
解答 解:同主族元素自上而下非金属性减弱,同周期元素自右到左非金属性减弱,所以非金属性C>Si,Cl>S>Si,碳原子的最外层是四个电子,Cl原子最外层是7个电子,得电子能力Cl>C,故选D.
点评 本题考查同主族、同周期元素性质递变规律,比较基础,注意理解掌握元素周期律是关键.

练习册系列答案
相关题目
18.两种气态烃组成的混合物1.12L(标准状况),完全燃烧后得到CO22.24L(标准状况)和1.8g水.该混合物的组成可能是( )
| A. | CH3OH和C3H4 | B. | CH4和C3H4O | C. | CH4和C2H4 | D. | CH4和C3H4 |
15.NA为阿伏加德罗常数的值.下列说法中,正确的是( )
| A. | 常温常压下,l.6gCH4中含有共价键总数为0.4NA | |
| B. | 常温常压下,2.24 L NO2气体中含有NO2分子数为0.1NA | |
| C. | 1 L0.lmol•L-1的醋酸中含有H十离子数为0.1NA | |
| D. | 铝热反应中1 molFe3O4完全反应,转移的电子数为6NA |
12.下列关于硫酸铜溶液和氢氧化铁胶体的说法中,正确的是( )
| A. | 前者是混合物,后者是纯净物 | |
| B. | 两者都具有丁达尔效应 | |
| C. | 分散质的粒子直径均在1~100nm之间 | |
| D. | 前者可用于杀菌,后者可用于净水 |
19.下列说法正确的是( )
| A. | 碘单质的升华过程中,只需克服分子间作用力 | |
| B. | NH4Cl属于离子化合物,该物质中只存在离子键 | |
| C. | 在N2、CO2和SiO2物质中,都存在共价键,它们都是由分子构成 | |
| D. | 金刚石和足球烯(C60)均为原子晶体 |
14.T℃时,将足量的BaSO4固体溶于一定量水中达到溶解平衡后,假定溶液体积不变的情况下,加入Na2CO3使c(CO32-)增大过程中,溶液中c(Ba2+)和c(SO42-)的变化曲线如图所示.则下列说法错误的是( )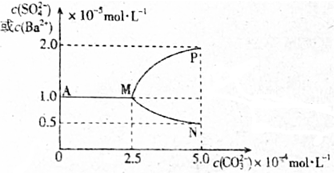

| A. | T℃时Ksp(BaSO4)<Ksp(BaCO3) | |
| B. | 当c(CO32-)大于2.5×10-4mol•L-1时开始有BaCO3沉淀生成 | |
| C. | 图象中代表沉淀转化过程中c(Ba2+)随c(CO32-)变化的曲线是MP | |
| D. | 反应BaSO4(s)+CO32-(aq)?BaCO3(s)+SO42-(aq)的平衡常数K=0.04 |

